
Faire des bébés : fonder une famille, la méthode HD
Faire des bébés : l’article de fond de HDBuzz – mis à jour pour 2024 – sur les technologies de fertilité qui peuvent aider les personnes à risque à avoir des enfants non atteints de la maladie de Huntington
Pour les personnes à risque de la maladie de Huntington, le fait d’avoir un bébé qui pourrait hériter de la MH peut rendre les décisions concernant la planification familiale extrêmement difficiles. Cet article explique les options disponibles et comment la science de la reproduction moderne peut faire une différence dès maintenant pour les familles touchées par la MH.
Avertissement concernant le contenu Cet article décrit des problèmes de fertilité, des choix difficiles et des procédures médicales, y compris l’interruption de grossesse.
Toutes les techniques décrites ici ne sont pas disponibles partout et, dans certains pays, elles peuvent entraîner des dépenses importantes. Donc, si vous envisagez l’une d’entre elles, nous vous recommandons de contacter un conseiller en génétique spécialisé pour obtenir des conseils personnalisés. Plus vous le ferez tôt, plus vous aurez d’options.

Introduction
Beaucoup de personnes atteintes de la maladie de Huntington, ou à risque de l’être, aimeraient savoir s’il existe des moyens d’avoir des enfants sans transmettre la maladie à la génération suivante. La réponse courte est oui !
La science génétique et les technologies de la reproduction signifient que plusieurs choix s’offrent aux personnes à risque de la maladie de Huntington, afin de garantir que les futurs enfants ne risquent pas de développer la MH. Cela inclut les personnes qui ont subi des tests et qui sont porteuses d’une expansion du gène HD, mais il peut également y avoir des options pour certaines personnes qui choisissent de ne pas passer elles-mêmes un test génétique HD.
Première chose : rien ne doit changer
Bien qu’une grande partie de cet article se concentre sur les options permettant d’avoir des enfants non atteints de la MH, il est important de savoir qu’avoir un enfant sans faire de test génétique est tout à fait une option pour les parents à risque de la maladie.
Comme le confirme chaque article de HDBuzz, les scientifiques font de réels progrès dans la recherche de traitements contre la maladie de Huntington. Bien que nous ne puissions rien garantir ni promettre un calendrier précis, nous croyons fermement qu’un jour viendra où les enfants à risque naîtront dans un monde où la MH est une maladie traitable.
De plus, il y a toujours une chance que l’enfant n’hérite pas de l’expansion du gène HD en premier lieu et, par conséquent, ne développe jamais la MH.
Certaines personnes peuvent vouloir garantir des enfants non atteints de la MH, mais des options peuvent ne pas être disponibles pour elles, par exemple en fonction de leur lieu de résidence, de leur soutien financier ou de leurs convictions religieuses.
Avoir un enfant à risque de MH est un sujet de discussion et de débat au sein de la communauté MH. Bien que les gens ne soient pas d’accord avec les décisions que prennent les autres, il est important de se rappeler que chacun a le droit d’être respecté lorsqu’il prend ses propres décisions.
L’Organisation de la jeunesse atteinte de la maladie de Huntington dispose de ressources pour aider à discuter de la MH et du risque génétique avec les enfants d’une manière adaptée à leur âge :
Certaines personnes estiment qu’elles ne veulent prendre aucun risque et qu’elles aimeraient éviter complètement le risque de transmettre la MH. C’est là que les techniques de test génétique entrent en jeu. Ces options sont disponibles, que ce soit vous ou votre partenaire qui soyez à risque de MH.
Quelles sont mes options de test génétique ?
Grâce aux tests génétiques, nous pouvons identifier le risque de MH pour un fœtus pendant une grossesse, ou dans des embryons en laboratoire.
Le test d’un fœtus pendant la grossesse est appelé test prénatal. Le test d’embryons en laboratoire est une forme de fécondation in vitro ou FIV, et est appelé test génétique préimplantatoire ou TGP.
Si vous ou votre partenaire avez subi un test génétique qui confirme que vous êtes porteur d’une expansion du gène HD, vous seriez en mesure de passer un test direct pendant la grossesse ou par le biais du TGP, afin de confirmer si la grossesse ou l’embryon a hérité ou non de l’expansion du gène HD.
Certaines personnes veulent des enfants non atteints de la MH sans passer elles-mêmes le test génétique. Il existe également des options pour cela ! Elles impliquent des versions plus compliquées des mêmes méthodes. Nous allons donc d’abord discuter de la façon dont cela fonctionne pour les couples où l’un des partenaires a déjà subi un test génétique HD positif.
Test génétique préimplantatoire (TGP)
Le test génétique préimplantatoire est un moyen d’avoir un enfant non atteint de la MH sans avoir à envisager l’interruption de grossesse. Il peut s’agir d’un processus long, difficile et coûteux.
Le TGP consiste à utiliser des ovules et des spermatozoïdes pour créer des embryons dans un laboratoire, puis à effectuer le test HD sur les embryons et à ne placer que les embryons HD négatifs dans l’utérus.
Le processus de TGP
Le TGP est une FIV avec une étape supplémentaire de test génétique. La FIV est une procédure médicale qui implique un médicament hormonal pour amener le fournisseur d’ovules à produire plus d’ovules que la normale. Les médicaments hormonaux peuvent impliquer des injections pour administrer les médicaments dans le corps.
Les ovules sont ensuite prélevés et fécondés à l’aide d’un échantillon de sperme.
Les ovules fécondés se développent en embryons, qui sont cultivés en laboratoire pendant cinq jours maximum jusqu’à ce qu’ils forment un petit amas de cellules. Une ou deux cellules sont prélevées sur chaque embryon à ce stade et envoyées pour un test génétique pendant que les embryons sont congelés et stockés. Le prélèvement de cellules à ce stade précoce du développement n’affecte pas la façon dont l’embryon se développe.
Tous les embryons qui ne présentent pas de risque de développer la MH continueront d’être stockés. Selon le pays dans lequel vous vous trouvez, un ou deux de ces embryons sans risque sont ensuite transférés dans l’utérus.
Environ deux semaines après le transfert des embryons, un test de grossesse est effectué sur un échantillon de sang. Si le transfert a réussi, la grossesse se déroule alors normalement.
L’inconvénient du TGP
Le processus de stimulation de la libération d’ovules, de prélèvement d’ovules, de fécondation à l’extérieur du corps et de retour des embryons dans l’utérus est toujours un processus long et épuisant. Il peut également être dangereux, car il comporte des risques que la personne tombe malade.
Diverses choses peuvent mal tourner, comme le fait de ne pas produire suffisamment d’ovules ou d’embryons. Il y a également plus de chances d’avoir des jumeaux avec le TGP, ce qui est plus difficile et plus risqué.
En plus des risques de la procédure, des choses peuvent mal tourner avec la partie génétique du TGP. Les embryons peuvent être endommagés lorsque des cellules sont prélevées, et parfois le test HD ne fonctionne pas parce qu’il n’y a pas assez d’ADN. La malchance peut signifier que tous les embryons ont la mutation HD.
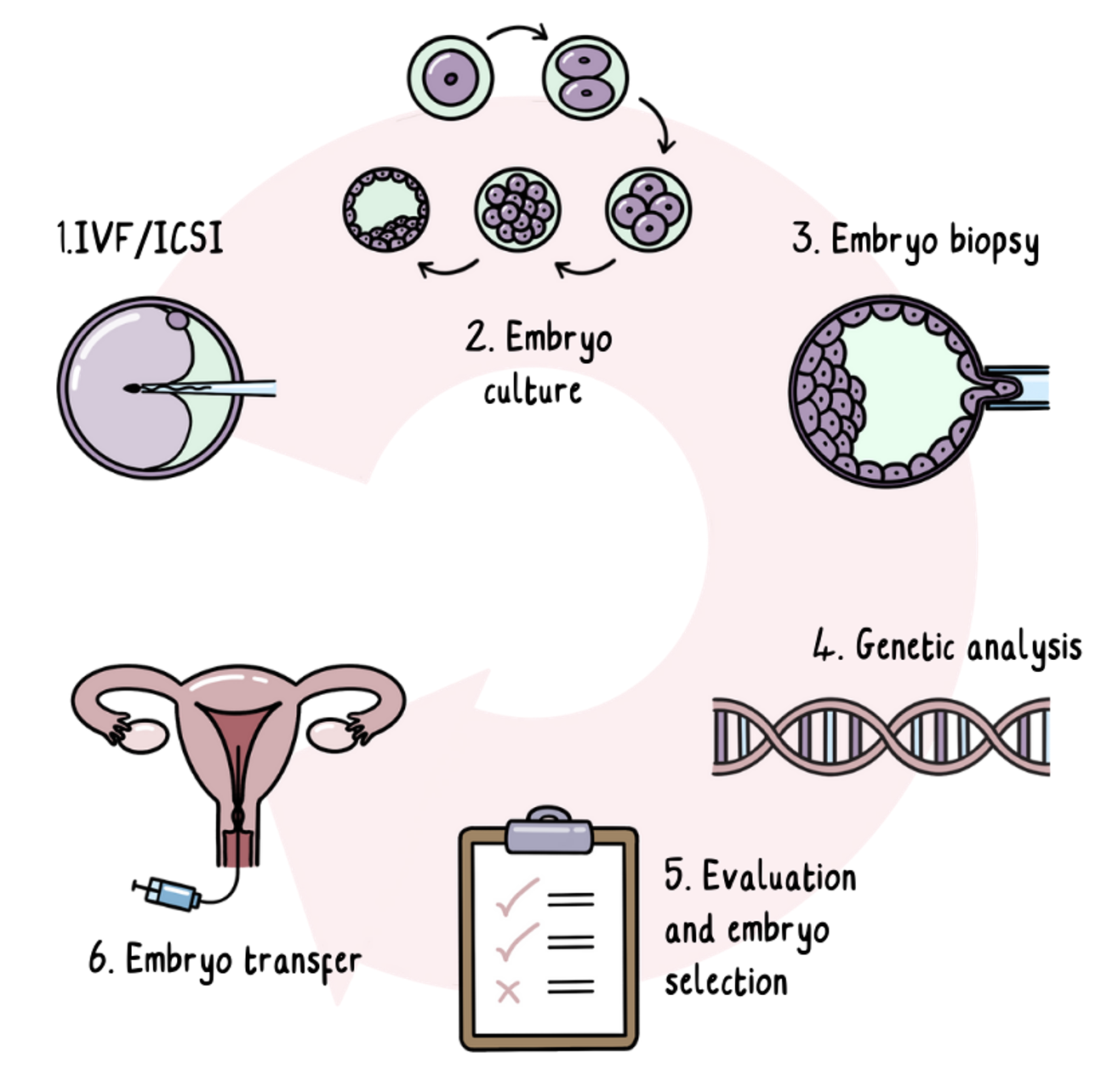
Crédit image : @gcnotes
En fin de compte, il arrive parfois qu’un seul embryon soit disponible pour l’implantation, et parfois aucun. Pour couronner le tout, une grossesse peut échouer après l’implantation. Dans l’ensemble, chaque tentative de TGP donne une chance de 20 à 30 % d’obtenir une grossesse sans MH. Ce taux de réussite varie selon le centre de TGP et dépend d’un certain nombre de facteurs.
Les femmes de moins de 35 ans ont les taux de réussite les plus élevés, une autre raison de penser à l’avenir en matière de fertilité. Malheureusement, les chances de succès au-delà de 40 ans sont faibles.
Combien coûte le TGP ?
Le TGP est coûteux. Le coût se situe aux alentours de 20 000 $ US (15 000 £ ou 18 000 €) pour chaque tentative.
L’assurance maladie ne couvre généralement pas le coût du TGP/DPI. Dans certains pays, le système de santé publique finance certaines tentatives de TGP – par exemple, trois tentatives au Royaume-Uni – mais même cela peut varier au sein des différents pays, et peut être limité aux couples sans enfants existants.
Tous les embryons supplémentaires qui ne présentent pas de risque de MH peuvent être stockés. Cependant, cela entraîne également un coût qui varie en fonction de la durée du stockage.
Si vous envisagez cette option, nous vous recommandons de contacter votre service de génétique local pour discuter de l’admissibilité, de l’orientation et des coûts associés.
Test pendant la grossesse
Il est possible d’effectuer un test génétique pendant la grossesse pour voir si le bébé en développement (fœtus) est porteur de l’expansion du gène qui cause la MH. C’est ce qu’on appelle le test prénatal.
Décider de tester ou non un fœtus est une décision difficile. Il est important de comprendre que le test prénatal de la MH n’est effectué qu’à la condition que si le résultat montre que le fœtus est porteur de l’expansion du gène HD, la grossesse sera interrompue. Il s’agit d’un choix extrêmement difficile et personnel.
Il est important de réfléchir attentivement au test prénatal de la MH et à ce que vous pensez de l’interruption de grossesse, avant de tomber enceinte.
Une fois enceinte, il y a très peu de temps pour absorber les informations sur le test prénatal et prendre ces décisions importantes, car le test doit être effectué tôt pendant la grossesse.
Tester une grossesse, mais ne pas procéder à une interruption après un résultat positif, priverait l’enfant du droit de choisir de passer ou non le test génétique, plus tard dans sa vie. Après tout, la plupart des personnes à risque de MH choisissent de ne pas passer le test avant de développer des symptômes. Nous savons que de gros problèmes peuvent survenir lorsqu’un enfant est identifié, dès la naissance, comme une personne qui développera la MH.
De plus, la plupart des tests de grossesse ne peuvent être effectués que si des tests ont été effectués au préalable sur le couple ou d’autres membres de la famille. Souvent, il n’y a pas assez de temps pour faire ce travail de fond lorsqu’une grossesse a déjà commencé.
Test prénatal invasif
Le plus souvent et le plus fiable, une procédure appelée prélèvement de villosités choriales ou PVC est effectuée au début de la grossesse pour tester le fœtus. Le PVC consiste à prélever un petit échantillon du placenta qui représente l’ADN du fœtus.
Le PVC est une procédure rapide en clinique externe et, dans certains pays, il est effectué sous anesthésie locale. Selon l’endroit où le placenta est attaché à la paroi de l’utérus, une très fine aiguille est passée soit par le col de l’utérus, soit par la peau de l’abdomen, à l’aide d’un échographe pour la guider. Un petit échantillon de cellules est ensuite prélevé sur le placenta.
Ces cellules peuvent être utilisées pour tester l’expansion du gène HD. Certains centres de génétique proposeront également des tests pour trois syndromes chromosomiques courants dans le cadre du test génétique PVC.
Le PVC est généralement effectué entre 11 et 12 semaines de grossesse, mais au plus tard à 15 semaines. Une échographie de datation précoce est souvent nécessaire avant qu’un PVC ait lieu.
La principale complication de cette procédure est un faible risque de fausse couche. Chaque centre disposera d’informations spécifiques sur le risque de fausse couche après un PVC. Veuillez contacter votre centre local si vous souhaitez en savoir plus.
Une amniocentèse est un autre type de technique de test prénatal invasif, similaire à un PVC, mais qui prélève un échantillon de liquide amniotique plutôt que de placenta. Elle peut être effectuée à partir de 16 semaines. Cela fournit donc un résultat à un stade de gestation beaucoup plus avancé et peut rendre les décisions concernant l’interruption de grossesse encore plus difficiles.
Si le test génétique est positif, une interruption peut généralement être pratiquée sous anesthésie générale jusqu’à environ 12 à 13 semaines, selon les lois du pays. Malheureusement, il peut parfois y avoir une liste d’attente pour cette procédure.
Dans certains pays, l’interruption de grossesse peut être pratiquée plus tard en induisant le travail ; toutefois, la disponibilité de cette option dépend également des lois du pays.
Que faire si je ne veux pas passer moi-même le test génétique ?
Il existe des moyens d’avoir des enfants non atteints de la MH sans que le partenaire à risque ne passe lui-même le test.
Ils utilisent les mêmes méthodes de base que nous avons décrites – test prénatal ou TGP – avec une touche génétique pour identifier les grossesses ou les embryons « à haut risque » sans révéler le statut du gène HD du partenaire à risque.
La touche est une paire de méthodes appelées test d’exclusion ou test de non-divulgation. Celles-ci impliquent plus de préparation et de planification, et il y a certaines situations où ce n’est pas possible, donc si cela vous semble être la bonne option : obtenez des conseils d’experts tôt.
Comment fonctionne le test d’exclusion ?
Le test d’exclusion implique au moins trois échantillons de sang. Un de chaque membre du couple qui souhaite agrandir sa famille et idéalement un de chaque parent de la personne à risque de développer la MH. Cette technique peut parfois ne pas être une option sans un échantillon de sang du parent atteint de la MH.
Nous savons que chacun d’entre nous héritera d’une copie du gène HD de chaque parent. Le grand-parent atteint aura une copie normale du gène HD et une copie étendue du gène HD. Nous pouvons étiqueter ces gènes « AA ». Nous ne savons pas lequel de ces gènes a été transmis à leur enfant adulte – et cette personne ne veut pas passer le test pour le savoir.
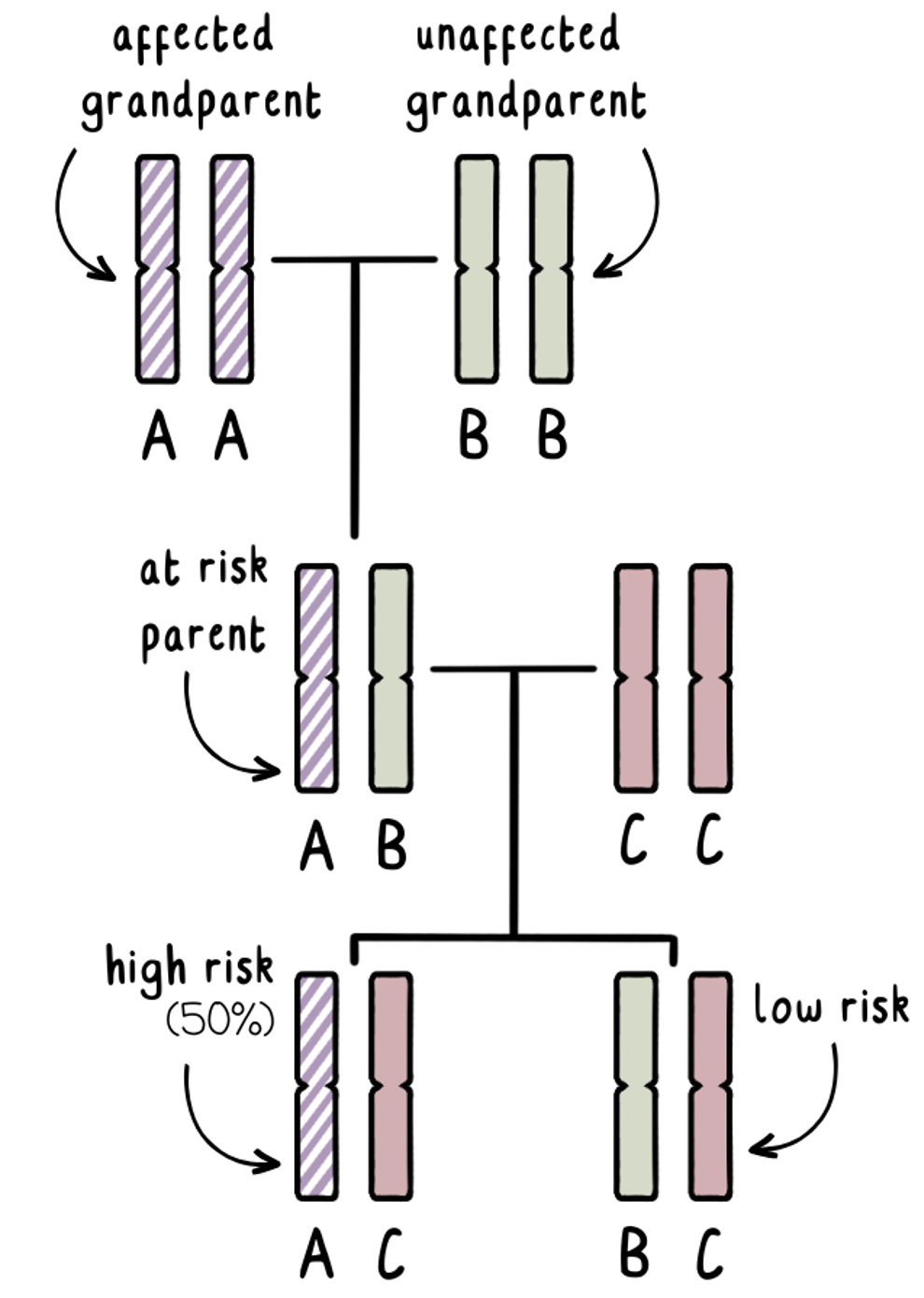
Crédit image : @gcnotes
Le grand-parent non atteint aura deux copies normales du gène HD. Nous pouvons les appeler « BB ».
L’adulte à risque aura une combinaison de A et de B, le gène A ayant une chance de 50 % de porter la mutation.
S’ils souhaitent avoir une famille sans passer de test génétique pour déterminer leur propre risque, nous pouvons utiliser le test d’exclusion lors d’un test prénatal ou d’un TGP pour identifier si le fœtus ou l’embryon a hérité d’un gène A du grand-parent atteint, ou d’un gène B du grand-parent non atteint. Cela nous indique si la grossesse serait à haut risque ou à faible risque.
Essentiellement, le test d’exclusion identifie le grand-parent d’origine, sans nous dire si le gène HD étendu a été hérité. Si nous découvrions la réponse à cette question, cela pourrait nous indiquer les résultats du parent à risque – ce que nous essayons d’éviter !
L’inconvénient est que certains embryons à haut risque ne portent pas de mutation HD, ce qui signifierait potentiellement mettre fin à une grossesse ou jeter des embryons qui n’auraient peut-être pas été à risque de MH en premier lieu.
TGP sans divulgation
La non-divulgation est une variante du TGP qui permet aux personnes à risque d’avoir des enfants non atteints de la MH sans connaître leur propre statut génétique. Cette option n’est pas disponible dans tous les pays, il est donc important de contacter votre service de génétique local pour savoir si cette option est disponible dans votre région.
Si un couple à risque opte pour le TGP sans divulgation, l’échantillon de sang de la personne à risque serait testé pour la mutation HD. La personne à risque ne serait pas informée du résultat de ce test, ni aucun des professionnels de la santé que la personne à risque rencontre – seuls les professionnels du laboratoire de fertilité connaîtraient le résultat.
Le TGP commence alors, avec le prélèvement d’ovules et la génération d’embryons. Si le résultat du test « secret » de la personne à risque montre qu’elle a une expansion du gène HD, les embryons sont testés pour la MH, et seuls ceux qui n’ont pas l’expansion du gène HD sont transférés pour une grossesse potentielle.
Le couple n’est pas informé du nombre d’ovules prélevés, du nombre d’ovules fécondés avec succès, ni du nombre d’embryons implantés. S’il n’y a pas d’embryons sans expansion du gène de la MH, le cycle s’arrête là, et on informe le couple que la fécondation a échoué, sans en préciser la raison.
La FIV peut échouer pour de nombreuses raisons, donc un échec de grossesse ne peut pas être interprété comme signifiant que la personne à risque est porteuse du gène de la MH.
Autres options
Une façon d’avoir des enfants sans MH est d’utiliser des ovules ou du sperme de donneur à la place de ceux de la personne à risque. Décider d’avoir un enfant avec l’aide d’un donneur est une décision difficile mais évite d’avoir à envisager l’interruption de grossesse. Cela peut se faire pour les personnes qui ont eu un test prédictif montrant qu’elles sont porteuses d’une expansion du gène de la MH, ainsi que pour celles à risque qui ne souhaitent pas être testées.
Comme tous les choix, c’est compliqué. L’enfant n’aura pas de lien génétique avec le parent à risque, et il faudra réfléchir attentivement à la façon et au moment de partager cette information avec l’enfant. Un parent n’a pas besoin d’être génétiquement lié à son enfant pour remplir pleinement son rôle parental avec amour. Il existe beaucoup de soutien disponible pour les personnes qui décident de suivre cette voie, et cela peut être discuté avant de s’engager dans le processus.
Beaucoup de couples envisagent l’adoption d’enfants. Dans de nombreux endroits, les couples dont l’un des partenaires est à risque de MH peuvent avoir des difficultés à adopter un enfant. Cela est dû à la présence de la maladie dans la famille et l’agence d’adoption doit s’assurer que l’enfant aura un foyer stable. Cependant, chaque cas est évalué individuellement, donc cela vaut la peine d’explorer l’adoption comme option. Si l’adoption vous a été refusée, les couples à risque peuvent devenir famille d’accueil pour des enfants, car c’est souvent une option à court terme, prenant soin des enfants pendant des semaines ou des mois. Même si le temps passé avec les enfants en famille d’accueil est court, il peut avoir un impact positif sur leur vie.
Orientations futures
Le diagnostic prénatal non invasif est une nouvelle façon de tester pendant la grossesse sans faire de test invasif, évitant ainsi le faible risque de fausse couche. Au lieu d’un test invasif qui prélève un échantillon du placenta ou du liquide amniotique, le DPNI prélève un échantillon de sang du parent portant la grossesse. Ce test recherche de minuscules fragments d’ADN du fœtus qui circulent dans le sang des parents.
Le DPNI peut avoir lieu à partir d’environ 10 semaines de grossesse. Il nécessite généralement un travail préparatoire du laboratoire avant une grossesse. Il requiert des échantillons du couple souhaitant agrandir sa famille et peut nécessiter un échantillon d’un parent atteint.
Le DPNI est déjà disponible en clinique pour certains troubles héréditaires et est en développement pour la MH mais n’est pas encore largement disponible. Il existe plusieurs cas où le DPNI ne serait pas approprié, par exemple lors de grossesses gémellaires. Si et quand le DPNI pour la MH sera disponible, il est probable qu’un résultat indiquant une grossesse à risque de MH soit encore suivi d’un test invasif pour confirmer les résultats, avant de programmer une interruption.
Qu’en est-il des personnes LGBTQIA+ ?
Toutes les options discutées ci-dessus sont probablement disponibles pour les couples LGBTQIA+ ayant des antécédents familiaux de MH et souhaitant fonder une famille. Il y aurait l’étape supplémentaire de trouver un donneur de sperme ou d’ovules ainsi qu’une mère porteuse, si nécessaire, ce qui impliquera des coûts et des formalités juridiques supplémentaires.
Dans de nombreux pays, être LGBTQIA+ ne t’empêchera probablement pas d’accéder à l’option de planification familiale qui te convient, à toi et à ton partenaire. Il existe des informations spécifiques sur les techniques de planification familiale disponibles dans ton pays pour les couples LGBTQIA+ qui souhaitent avoir une famille.
Résumé
Il existe plusieurs options disponibles pour les personnes à risque de MH qui souhaitent fonder une famille.
Tout le monde ne choisit pas de passer par des tests génétiques pour fonder une famille, et c’est une option tout à fait valable.
Pour ceux qui souhaitent éliminer le risque que leur enfant hérite de la MH, ils n’ont pas nécessairement besoin de connaître leur propre risque de MH. Le test direct peut avoir lieu lorsque nous connaissons le résultat du parent à risque et qu’il est démontré qu’il a l’expansion du gène de la MH. En revanche, les tests d’exclusion ou de non-divulgation peuvent être effectués pour les couples à risque qui ne souhaitent pas connaître leurs propres résultats.
Les tests directs et de non-divulgation peuvent avoir lieu pendant le test génétique préimplantatoire (TGP) où les embryons sont créés en laboratoire et testés pour leur risque de développer la MH, ou un fœtus peut être testé pendant la grossesse. Les tests pendant la grossesse peuvent être invasifs via le prélèvement de villosités choriales (PVC) ou non invasifs (DPNI), mais ces deux options ne sont disponibles que pour ceux qui envisageraient d’interrompre une grossesse à risque de développer la MH.
Il existe d’autres options disponibles pour les couples à risque, notamment l’utilisation d’ovules/sperme de donneur ou l’adoption/le placement en famille d’accueil d’enfants.
Les conseils d’experts, sous forme de conseil génétique, t’aideront à comprendre les options exactes disponibles localement et à explorer quelle option te semble la plus appropriée. L’Association MH de ton pays peut t’indiquer comment contacter un conseiller en génétique. Comme pour tant de choses dans la vie, la planification à l’avance et la compréhension de toutes les options sont essentielles.
En savoir plus
- Page de Genetic Alliance (UK) sur le test génétique préimplantatoire
- National Society of Genetic Counselors (USA). Trouvez un conseiller en génétique en ligne. Votre médecin généraliste ou l’Association régionale de la MH peut également vous conseiller pour être orienté vers un conseiller en génétique pour discuter des options de fertilité.
- Guide de l’Autorité de la fertilité humaine et de l’embryologie sur la fertilité assistée pour les personnes vivant avec des conditions génétiques (UK)
Sources et références
Pour plus d’informations sur notre politique de divulgation, consulte notre FAQ…


