Découvertes éclairantes dans les cellules sanguines de patients atteints de la maladie de Huntington
Les niveaux de la protéine huntingtine peuvent être mesurés directement dans le sang – cela pourrait-il être utile pour les études de silençage génique ?

Avec les thérapies de silençage génique qui se dirigent vers la clinique, une nouvelle question s’est posée : comment saurons-nous si elles fonctionnent ? Comment pouvons-nous savoir si la quantité de protéine huntingtine est réduite chez les personnes ? De nouveaux travaux menés à Londres et à Bâle démontrent que la protéine huntingtine est détectable dans des échantillons de sang et que ses niveaux changent au cours de la maladie de Huntington.
Pourquoi la mesure est-elle si importante ?
L’une des idées les plus fondamentales de la science est que nous devons être capables de mesurer quelque chose avant de pouvoir l’étudier. Comment savons-nous si un médicament fonctionne ? Nous le donnons à un groupe de personnes, nous donnons à un autre groupe de personnes très similaire une pilule de sucre (« placebo »), puis nous mesurons un symptôme chez les deux groupes de personnes. Le médicament est efficace si les personnes qui ont reçu le médicament se portent mieux que celles qui ont reçu le placebo.
Des études comme PREDICT-HD, TRACK-HD et d’autres nous ont appris énormément de choses sur ce qui arrive aux personnes au cours de la maladie de Huntington. Nous sommes prêts, essentiellement, à choisir des ensembles de symptômes afin de pouvoir mesurer si de nouveaux médicaments sont efficaces ou non.
Mais, à un niveau plus profond – un scientifique dirait au niveau moléculaire – comment savons-nous qu’un médicament agit de la manière dont nous pensons qu’il devrait agir ? Dans certains cas, nous pouvons réellement mesurer directement les actions des médicaments.
Par exemple, des millions de personnes prennent des médicaments appelés statines qui préviennent les crises cardiaques en réduisant le taux de cholestérol dans le sang. Nous pouvons dire qu’une statine fonctionne, sans attendre les crises cardiaques, en mesurant simplement le taux de cholestérol dans le sang.
Chaque patient atteint de la maladie de Huntington est porteur de la même mutation dans son ADN – un bégaiement génétique près d’une extrémité d’un gène que nous appelons le gène HD. Les gènes sont utilisés par les cellules comme plans pour créer des protéines – les machines qui effectuent la plupart des travaux importants de nos cellules. Le gène HD indique donc au corps comment fabriquer une protéine que nous appelons de manière quelque peu déroutante « huntingtine ».
L’une des thérapies les plus prometteuses contre la maladie de Huntington est le silençage génique, qui vise à réduire les niveaux de la protéine HD (huntingtine) dans le cerveau des personnes porteuses de la mutation HD. Parce que nous savons que chaque personne atteinte de la maladie de Huntington a une mutation dans le même gène, il est facile d’imaginer que cette approche serait efficace.
Mais comment saurons-nous si les médicaments que nous concevons pour faire taire le gène HD fonctionnent réellement ? Chez les souris et autres organismes, nous pouvons simplement prélever des échantillons de cerveau sur des animaux après leur mort et mesurer les niveaux de la protéine huntingtine avec des techniques de laboratoire standard.
Mais il n’y a aucun moyen de prélever des échantillons de tissu cérébral sur des personnes participant à un essai de silençage génique. Il serait idéal de pouvoir mesurer les niveaux de la protéine huntingtine dans des échantillons faciles à collecter, comme le sang.
Un groupe de scientifiques dirigé par le professeur Sarah Tabrizi de l’University College London et le Dr Andreas Weiss de la société pharmaceutique Novartis a entrepris d’utiliser une technique développée chez Novartis pour mesurer la protéine HD dans le sang de volontaires de l’étude TRACK-HD.
Une nouvelle technique permet de poser de nouvelles questions
L’équipe a utilisé une technique très sensible appelée « Transfert d’énergie par résonance de fluorescence résolue dans le temps » ou TR-FRET. La technique utilise une paire d’anticorps – qui sont des protéines qui se fixent à une autre protéine spécifique – pour marquer la huntingtine.
Les détails techniques sont extrêmement compliqués, mais l’idée de base est que lorsque vous frappez l’un des anticorps avec une certaine fréquence de lumière, cela provoque l’émission par l’autre anticorps d’une lumière d’une fréquence différente. L’intensité de cette fréquence de lumière différente nous indique la quantité de protéine huntingtine présente. L’avantage de cette approche est qu’elle est très sensible, ce qui permet à l’équipe de mesurer les niveaux de protéine huntingtine à partir de très petits volumes d’échantillons biologiques, tels que le sang.
L’équipe de Tabrizi s’intéresse depuis longtemps à l’activation du système immunitaire dans la maladie de Huntington. Ils ont publié des travaux démontrant que le système immunitaire des patients atteints de la maladie de Huntington semble être hyperactif. Cela peut sembler une bonne chose, mais les scientifiques savent qu’une activation excessive du système immunitaire peut être mauvaise – et pourrait même affecter les événements qui se produisent dans le cerveau.
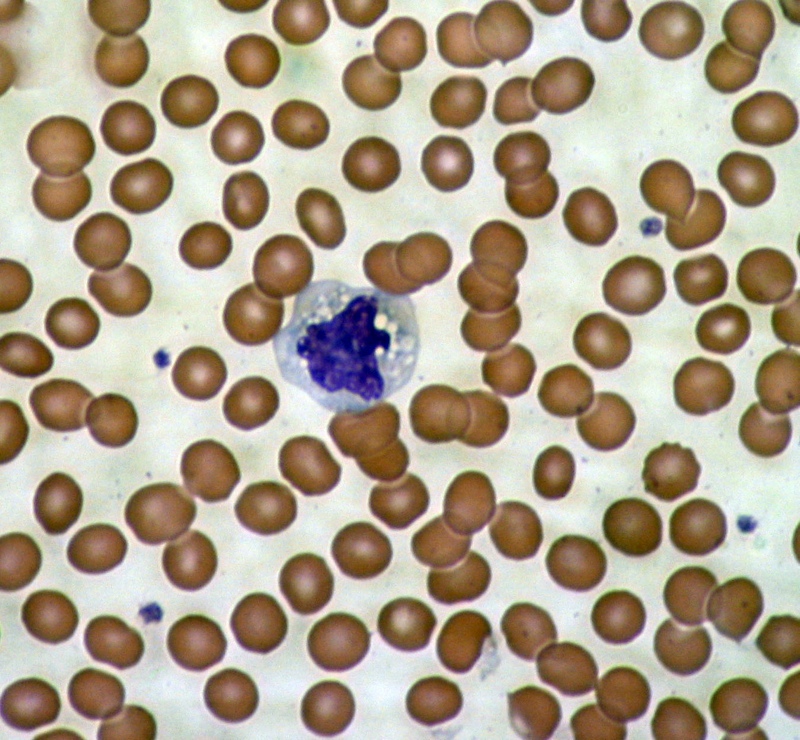
Compte tenu de cet intérêt et de la capacité de mesurer la protéine huntingtine à partir de petits échantillons, l’équipe a entrepris de mesurer la quantité de protéine huntingtine présente dans différents types de cellules du sang de patients atteints de la maladie de Huntington. Étant donné que le système immunitaire est en grande partie composé de cellules circulant dans le sang, ils ont pensé que la mesure des niveaux de huntingtine à cet endroit pourrait être utile.

Qu’ont-ils découvert ?
Ce qu’ils ont découvert est intéressant et un peu déroutant. Dans différents types de cellules immunitaires, ils ont constaté que les niveaux globaux de la protéine huntingtine étaient inchangés à mesure que la maladie de Huntington progressait. Il s’agit d’une démonstration utile de leur technique, qui montre qu’ils peuvent mesurer avec précision les niveaux de la protéine huntingtine dans les cellules à partir de petits échantillons de sang.
L’équipe a ensuite utilisé différents anticorps dans ses mesures, de sorte qu’ils ne reconnaissaient que la forme mutante de la protéine huntingtine. N’oubliez pas que la grande majorité des patients atteints de la maladie de Huntington (et tous les participants à cette étude) ont deux types de protéine huntingtine : normale et mutante.
Lorsqu’ils ont mesuré uniquement la forme mutante de la protéine HD, l’équipe a observé des signaux accrus chez les personnes qui avaient présenté des symptômes de la maladie de Huntington plus longtemps. Il semble donc que les personnes atteintes d’une maladie de Huntington plus avancée ont plus de huntingtine mutante dans leurs cellules immunitaires dans le sang. Cette découverte est un peu surprenante, mais devrions-nous nous soucier de comprendre ce qui se passe ?
Connexions cerveau/corps
C’est là que réside la puissance des études observationnelles. Étant donné que l’équipe a examiné les volontaires qui ont donné ces échantillons de sang, elle a pu rechercher des corrélations entre ce qui se passait dans leur sang et la façon dont les personnes se portaient en termes de symptômes de la maladie de Huntington.
Ce qu’ils ont constaté, c’est que des niveaux plus élevés de protéine huntingtine mutante dans les cellules immunitaires du sang étaient clairement liés à une charge de symptômes plus élevée, et également associés à une atrophie cérébrale croissante. Ainsi, quoi qu’il en soit qui entraîne l’augmentation des niveaux de protéine huntingtine mutante dans les cellules sanguines, il vaut probablement la peine de le comprendre et cela pourrait nous apprendre quelque chose d’important.
Des expériences de suivi suggèrent que ce qui pourrait réellement s’accumuler dans les cellules sanguines des patients atteints de la maladie de Huntington, ce sont de courts fragments de la protéine huntingtine plus grande. Des travaux antérieurs de plusieurs laboratoires révèlent que la protéine huntingtine est découpée en petits morceaux et que ces petits morceaux pourraient être particulièrement toxiques pour la cellule.
En quoi est-ce utile ?
Ce travail est scientifiquement intéressant car il suggère qu’il pourrait y avoir une accumulation et une fragmentation de la protéine huntingtine dans les cellules immunitaires du sang des patients atteints de la maladie de Huntington. Il reste encore quelques mystères : que fait la protéine huntingtine normale dans ces cellules immunitaires ? L’accumulation de protéine huntingtine mutante est-elle liée à l’activation accrue du système immunitaire chez les patients atteints de la maladie de Huntington ?
En termes d’avantages immédiats, cette étude démontre qu’il est pratique de mesurer les niveaux de protéine huntingtine normale et mutée à partir de très petits échantillons, ce qui constitue une avancée technique importante qui aura de nombreuses utilisations dans la recherche sur la maladie de Huntington. De plus, cette technique pourrait être utilisée pour suivre les niveaux de protéine huntingtine mutante dans le sang, ce qui pourrait fournir un outil utile aux scientifiques qui conçoivent des essais de médicaments, en particulier ceux qui se concentrent sur le silençage génique.
Une possibilité très intéressante qui doit être étudiée plus avant est de savoir si les niveaux de protéine huntingtine mutante dans le sang reflètent les niveaux de huntingtine mutante dans le cerveau – en substance, cela offre-t-il une fenêtre sur ce qui se passe dans le cerveau ? Si c’est le cas, cela pourrait être une jauge très utile pour déterminer si les thérapies qui visent à réduire les niveaux de la protéine huntingtine mutante dans le cerveau fonctionnent réellement.
En savoir plus
Pour plus d’informations sur notre politique de divulgation, consulte notre FAQ…


