Une nouvelle étude nous éclaire sur la dégénérescence régionale dans la MH
Pourquoi certains neurones meurent dans la MH? Une nouvelle étude suggère un lien avec leur efficacité à recycler.
Par Dr Kurt Jensen 11 avril 2014 Edité par Dr Jeff Carroll Traduit par Laurie Galvan Initialement publié le 12 novembre 2013
Certaines régions du cerveau dégénèrent plus vite que d’autres dans la maladie de Huntington. L’équipe de Steven Finkbeiner a montré que cette différence est basée sur la variabilité d’aptitude des cellules de ces régions du cerveau, d’identifier et d’éliminer la protéine mutante HD. Plus précisément, les neurones des régions les plus vulnérables sont les plus lents à éliminer cette protéine.
Savoir comment les plier
Les protéines sont de grosses molécules biologiques qui exécutent divers mais essentiels travaux pour la cellule. Quant une protéine est créée par un assemblage ordonné d’acides aminés, elle se met à se plier un peu comme un Bretzel afin de créer une forme unique en trois dimensions. C’est seulement quand la protéine est pliée correctement qu’elle peut accomplir son travail.
Malheureusement, certaines protéines s’abiment en chemin et ne peuvent plus être pliées correctement. Dans la MH, la mutation génétique affecte un des acides aminés de la chaine d’assemblage de la protéine huntingtine (Htt) de manière à ce qu’il soit répété encore et encore, comme un tourne disque raillé (ou comme un bégaiement si vous être trop jeune pour connaitre les tourne-disques).
Cette expansion/répétition produit un mauvais repliement de la Htt, qui devient toxique pour la cellule, et s’agrège les unes aux autres en tas, que les scientifiques appellent “agrégats”. Une bonne illustration pour cela est la boule de cheveux dans le drain de la douche : les cheveux seuls sont ok mais ensemble ils forment un amas qui bloque tout.
Chez les patients atteints de la MH, chaque cellule du corps semble exprimer la protéine Htt mutante mais ce sont les cellules du cerveau qui préférentiellement meurent pendant la progression de la maladie. C’est pourquoi on parle de maladie « neurodégénèrative ». En réalité, il n’y a pas que les cellules du cerveau qui meurent mais ce sont elles qui meurent précocement et donc semblent être vulnérables.
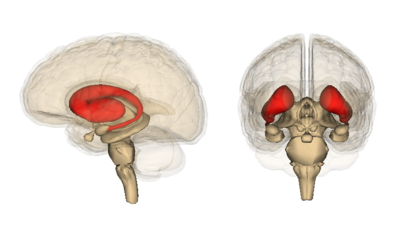
La région du cerveau qui montre une perte massive et précoce des cellules/neurones est appelé le striatum. Le striatum est localisé au centre du cerveau. Son job est de coordonner les mouvements volontaires, les pensées, les interactions sociales et s’assurer que les choses ne soient pas hors de contrôles.
Se figer sur place, arrêter une conversation ou un mouvement est du ressort du striatum. Ce qui est extrêmement important mais pas actuellement compris, c’est pourquoi cette région est susceptible à la dégénérescence dans HD alors que d’autres régions semblent s’en sortir bien mieux, et plus longtemps dans la gestion de la Htt mutante avant de mourir.
«Les neurones surchargés avec Nrf2 ont éliminé plus rapidement la Htt mutante qu’à la normale et ils ont été moins susceptibles de mourir. Cela suggère donc, que favoriser la voie de recyclage pourrait être une cible thérapeutique potentielle pour HD. »
Sortez les papiers, les poubelles et la huntingtine mutante
Deux explications possibles pour cette différence ont été explorées par l’équipe de recherche du Dr. Steven Finkbeiner à l’Université de Californie à San Francisco. La première réside dans la variabilité du taux d’assemblage de la Htt mutante chez les différentes cellules du cerveau. Pour reprendre notre image, à quelle vitesse les cheveux s’assemblent pour former une boule dans la douche ?
Une autre possibilité pour expliquer cette perte sélective de cellules, est que ces régions du cerveau éliminent ou disposent de manière différente la htt mutante. Est-ce que certaines cellules sont des pro du nettoyage ?
Les auteurs ont conçu une technique pour leur permettre de mesurer les propriétés d’assemblage et d’élimination chez des cellules du cerveau en culture. Elles ont été remplies avec une protéine fluorescente appelée « Dendra2 ». Cette protéine est super cool parce qu’elle fluoresce, d’abord dans le vert (comme les bâtons lumineux qu’on donne aux enfants) puis lorsqu’elle est illuminée par une couleur spéciale, elle fluoresce en rouge.
Cet outil nous permet de faire pousser des neurones remplis de dendra2 verte puis après les avoir illuminés, la dendra2 devient rouge. Le but est d’observer comment de temps va mettre la cellule pour produite un nouveau stock de protéines dendra2 vertes mais surtout, combien de temps il lui faut pour se débarrasser des vieilles protéines dendra 2 rouges.
A l’évidence on se soucie peu de dendra2. Ce qui est vraiment important c’est de savoir comme les cellules du cerveau gèrent la protéine normale Htt et si cette gestion est modifiée par la mutation causée dans la maladie de Huntington. Pour réponde à cette question, les scientifiques ont utilisés une astuce qui consiste à fusionner la protéine Htt normale et mutante avec la protéine dendra2. Maintenant ils peuvent utiliser la même astuce du changement de couleur pour étudier le devenir de la protéine Htt.
Equipe de nettoyage professionnelle
En utilisant ce système, ils ont remarqué que la protéine Htt mutante était éliminée des neurones du striatum plus rapidement que la Htt normale. Çà c’est une surprise…… nombreux scientifiques auraient prédit l’inverse en pensant que la forme mutante resterait plus longtemps ce qui causerait son accumulation en agrégat. Cela suggère que les neurones sont capables de reconnaitre la protéine mutante et la cibler pour élimination.
De plus, le microscope automatisé que l’équipe de Finkbeiner a développé, leur a permis de voir que le plus rapidement une cellule élimine la Htt mutante, le plus longtemps elle survit. Ce qui a du sens, nettoyer ce qui toxique protège les cellules du cerveau.
Donc si une cellule a un système de détection de protéine mutante et aussi de quarantaine, où est le problème ? Il s’avère que certains neurones sont meilleurs pour nettoyer que d’autres, comme ceux du cortex. Le cortex est la région plissée à l’extérieur du cerveau. En général, les cellules du cortex succombent à la MH bien après celles du striatum. Dans l’espoir de comprendre pourquoi, les auteurs ont comparé l’élimination de la protéine mutante dans HD dans le striatum versus le cortex.
«La principale découverte mentionnée dans cet article est le fait que les neurones de différentes régions du cerveau présentent une variabilité de vulnérabilité vis à vis de la Htt mutée.Cela pourrait expliquer pourquoi la maladie démarre dans un endroit du cerveau et pas dans un autre. »
Les neurones du cortex ont été capables de se débarrasser de la Htt mutante bien plus rapidement. Les neurones du cortex vivent plus longtemps que ceux du striatum. Les auteurs conclurent que la variabilité observée dans différentes régions du cerveau dans le processus d’élimination de la htt mutante pourrait être imputée aux propriétés intrinsèques de leurs systèmes de recyclage.
Quand les protéines deviennent vieilles et se désagrègent, la cellule dispose d’un système pour les recycler. Les chercheurs ont exploré si ces observations pouvaient être expliquées en modifiant le système de dégradation. En particulier, ils ont focalisés leur attention sur Nrf2, une protéine qui active la voie de recyclage.
Les scientifiques peuvent étudier comment un processus cellulaire contribue à un effet comme la mort de cellule ou le recyclage en augmentant le volume de production ou en le supprimant. Dans ce cas, parce qu’ils ont cru que le programme de recyclage enclenché par Nrf2 était important, ils ont donné aux cellules plus de Nrf2 ou l’ont enlevé. Cette astuce aide à établir ce qui est important dans le processus de recyclage.
C’est exactement ce qu’ils ont fait pour étudier Nrf2 et le recyclage de la Htt mutante. Les neurones surchargés avec Nrf2 ont éliminé plus rapidement la Htt mutante qu’à la normale et ils ont été moins susceptibles de mourir. Cela suggère donc, que favoriser la voie de recyclage pourrait être une cible thérapeutique potentielle pour HD.
Réciproquement lorsque les scientifiques réduisent artificiellement les déchets des cellules ou diminuent leur recyclage avec des traitements, les cellules sont moins capables de se débarrasser de la Htt mutante. Cette voie de recyclage semble donc être cruciale pour les neurones afin de gérer la protéine toxique.

Qu’est que cela signifie pour HD ?
La principale découverte mentionnée dans cet article est le fait que les neurones de différentes régions du cerveau présentent une variabilité de vulnérabilité vis à vis de la Htt mutée. Cela pourrait expliquer pourquoi la maladie démarre dans un endroit du cerveau et pas dans un autre. Le fait le plus intéressant est que cette vulnérabilité semblerait être basé sur les différentes capacités des neurones à gérer et dégrader les protéines mutantes plutôt que la toxicité intrinsèque de ces protéines.
Cela est très important car l’aptitude des neurones à gérer la protéine Htt mutante ouvre de nouvelles voies à de potentielles thérapies. En se basant sur cette étude, nous pouvons faire l’assomption qu’un traitement boostant la capacité des neurones à dégrader la protéine Htt mutant devrait aider les neurones à vivre plus longtemps.
Cependant, nous devons envisager cette possibilité dans son contexte. Premièrement, cette étude a été réalisée entièrement en utilisant des neurones qui ont grandit dans une boite à Pétri. Il reste à déterminer si le même phénomène peut être observé dans un cerveau humain malade.
Secondairement, ces découvertes sont préliminaires et les thérapies décrites tantôt n’existent pas encore. Cela va prendre du temps pour trouver un composé intéressant et le tester dans d’autres modèles de la MH avant qu’il soit amené chez l’humain. Par exemple, personne ne sait quels sont les effets secondaires de l’activation artificielle de Nrf2 sur du long terme.
Ces observations sont très intéressantes dans le contexte de la science fondamentale dans la MH. Il n’y a pas à ce jour, de traitements curatifs de la maladie de Huntington, des études comme celles-ci fournissent une meilleure compréhension des mécanismes de cette maladie et aident à éclairer la voie pour le développement de nouveaux traitements.


