
Un médicament recyclé nous donne un nouvel aperçu de la MH
Un médicament existant pourrait donner un coup de boost aux cellules cérébrales de la MH – mais il faudra peut-être plus de tests avant de retourner en clinique

Des chercheurs ont trouvé un lien entre la MH et une protéine régulatrice d’énergie appelée PPAR-delta. Stimuler le PPAR-delta avec un médicament existant s’est avéré protecteur dans les cellules et les souris MH, mais il faudra probablement plus de recherches et de tests avant de pouvoir l’utiliser en clinique pour la MH.
Réutilisation de thérapies
Parfois, un nouveau médicament prometteur s’avère sûr à utiliser chez l’homme, mais pas utile pour traiter la maladie pour laquelle il a été conçu. Dans ce cas, les scientifiques peuvent le ramener au laboratoire, effectuant de nouveaux tests sur des cellules et des souris pour mieux comprendre sa fonction. Finalement, ces connaissances pourraient conduire à la réutilisation d’un médicament sûr pour traiter une maladie différente.

Récemment, un médicament contre le diabète sûr mais mis de côté a été exploré dans des expériences liées à la maladie de Huntington. Le médicament agit sur une protéine trouvée dans la plupart des types de cellules appelée
Cette nouvelle recherche sur la MH confirme à quel point le PPAR-delta est important pour alimenter des cellules cérébrales saines – et montre que la mutation MH peut interférer avec la façon dont le PPAR-delta fait son travail. Dans les cellules et les souris MH, l’utilisation d’un médicament pour donner un « coup de boost » au PPAR-delta a favorisé des cellules plus saines et a conduit à des améliorations du comportement. C’est excitant, mais plus de tests sont probablement nécessaires avant de pouvoir le tester chez les patients MH.
Le PPAR-delta est un important facteur de transcription
Les scientifiques de la MH se sont intéressés au PPAR-delta car c’est une protéine avec un important travail de gestion dans les cellules. Comme le personnel d’une grande entreprise, chaque protéine dans une cellule fonctionne dans une délicate hiérarchie de coordination et de contrôle.
Certaines protéines accompagnent et supervisent d’autres en petits groupes, d’autres supervisent ces superviseurs, et sont à leur tour gérées par des directeurs de branche, et ainsi de suite jusqu’au PDG. Les cellules n’ont pas vraiment de PDG, mais les hauts responsables détiennent les clés du noyau, le centre de contrôle de la cellule, où l’ADN est stocké.
« Fait intéressant, l’anatomie et le comportement des souris sans PPAR-delta dans le striatum étaient quelque peu similaires aux souris MH – elles avaient des dommages striataux et des difficultés avec les tâches motrices et cognitives. Donc, avoir moins de PPAR-delta dans le striatum est une mauvaise nouvelle, et les conséquences de cette perte ressemblent un peu à la MH chez la souris »
Le PPAR-delta est une cible intéressante pour la recherche sur la MH car c’est l’un de ces hauts responsables : une protéine appelée facteur de transcription. Ces protéines initient et coordonnent le processus de transformation du « plan » génétique de l’ADN en une protéine fonctionnelle, décidant efficacement quelles protéines doivent être construites pour que la cellule fonctionne correctement.
Quand une protéine comme le PPAR-delta est au centre de l’action de nombreux autres éléments dans une cellule fonctionnelle, on l’appelle parfois un « régulateur maître ». En raison de sa position clé dans la coordination de la santé cellulaire, un facteur de transcription fortement lié à la MH pourrait avoir un bon potentiel comme cible médicamenteuse.
PPAR-delta et MH en laboratoire
Un groupe de scientifiques de l’Université de Californie à San Diego, dirigé par Albert La Spada, étudie le rôle des facteurs de transcription dans la MH depuis de nombreuses années. Pour leur publication la plus récente, ils ont testé de nombreux facteurs de transcription pour voir lesquels interagissent généralement physiquement avec la protéine huntingtine, et le PPAR-delta en faisait partie. Mais pourquoi se concentrer sur celui-ci ?
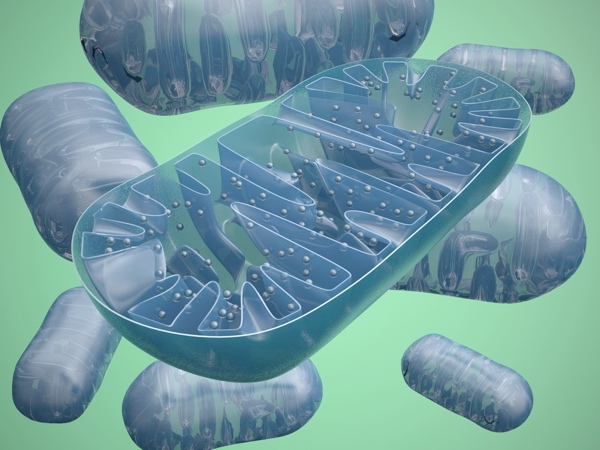
Le PPAR-delta est responsable d’une branche d’opérations qui construisent et maintiennent les mitochondries, les centrales énergétiques de la cellule. Les cellules cérébrales ont un métabolisme élevé, elles ont donc besoin de beaucoup d’énergie pour survivre. Les cellules d’une partie du cerveau appelée le striatum, celles qui sont affectées en premier et le plus fortement dans la MH, sont particulièrement vulnérables aux problèmes de mitochondries, donc le PPAR-delta pourrait être particulièrement important là-bas.

Crédit image : Protein Data Bank
L’équipe de La Spada a expérimenté avec des protéines et des cellules en laboratoire pour montrer que la protéine huntingtine et le PPAR-delta s’attachent directement l’un à l’autre, une bonne indication qu’ils pourraient travailler ensemble dans les cellules. Fait important, ils ont également constaté que la mutation MH conduit à des niveaux plus bas de PPAR-delta, et que cela perturbe l’entretien des mitochondries, contribuant aux dommages et à la mort cellulaire.
Les chercheurs ont pu corriger les neurones MH endommagés (toujours en laboratoire) en les traitant avec un agoniste du PPAR-delta – un médicament qui « booste » l’action du PPAR-delta, le rendant plus efficace pour réguler l’énergie. Ce médicament, appelé KD3010, a été développé par une entreprise de biotechnologie aujourd’hui disparue comme traitement du diabète. Lorsque le KD3010 a été administré aux cellules MH en laboratoire, il semblait bien protéger leurs mitochondries des dommages causés par la MH.
Passage aux mammifères
Le groupe de recherche de San Diego a effectué de multiples expériences sur des cellules et des souris pour montrer que le PPAR-delta est important pour les mitochondries et essentiel pour la santé du cerveau. C’est une contribution importante en soi, mais ils voulaient examiner de plus près le lien entre le PPAR-delta et la MH.
Pour étudier cela, ils ont utilisé une technique génétique pour supprimer le PPAR-delta uniquement des cellules du striatum, celles qui sont les plus susceptibles d’être endommagées dans la MH. En d’autres termes, l’activité cellulaire peut-elle encore fonctionner lorsqu’un directeur important démissionne ? Et comment cela affecte-t-il l’organisme entier ?
« Néanmoins, si le KD3010 résiste à plus d’expérimentation, il serait beaucoup plus facile de le transférer en clinique pour la MH, car nous savons déjà qu’il est sûr pour les humains »
Fait intéressant, l’anatomie et le comportement des souris sans PPAR-delta dans le striatum étaient quelque peu similaires aux souris MH – elles avaient des dommages striataux et des difficultés avec les tâches motrices et cognitives. Donc, avoir moins de PPAR-delta dans le striatum est une mauvaise nouvelle, et les conséquences de cette perte ressemblent un peu à la MH chez la souris. Cela soutient l’idée que la perte de certaines fonctions du PPAR-delta pourrait contribuer à la MH, et que stimuler le PPAR-delta pourrait être une bonne stratégie pour la MH.
L’étape suivante consistait à tester le médicament améliorant le PPAR-delta, le KD3010, chez les souris MH, pour voir s’il pouvait donner un coup de boost au cerveau MH. Chez les souris traitées au KD3010, les chercheurs ont observé des neurones plus sains dans le striatum, de légères améliorations des comportements moteurs, et les souris avaient une durée de vie légèrement plus longue.
Potentiel pour la clinique – peut-être
Le PPAR-delta et son agoniste KD3010 ont fait sensation dans les médias récemment car il est excitant quand un médicament sûr montre des résultats prometteurs dans les cellules et les souris. Mais l’engouement pour un possible essai clinique dans quelques années devrait être considéré avec prudence. Bien que cette recherche ait fait un grand pas en avant dans notre compréhension de ce que fait le PPAR-delta dans le cerveau, le lien avec la MH doit être confirmé avant que nous commencions à tester le KD3010 chez les personnes porteuses de la mutation.
De ce travail récent, voici ce que nous savons. Premièrement, le PPAR-delta est définitivement important pour un cerveau fonctionnel, et il interagit directement avec la protéine huntingtine. Deuxièmement, nous savons que la huntingtine mutante altère le PPAR-delta, de sorte qu’il ne peut pas remplir correctement sa fonction importante. Troisièmement, augmenter le PPAR-delta dans les cellules MH peut les protéger et protéger la santé de leurs mitochondries.
Mais quant à l’utilisation du KD3010 comme traitement dans un avenir proche, il y a quelques limites à considérer. Les chercheurs n’ont testé le médicament que sur un seul type de modèle de souris MH, et ont observé des améliorations relativement légères du comportement. Même si ce travail a révélé des liens importants entre le PPAR-delta et la protéine huntingtine, il pourrait ne pas être utile de commencer à tester un médicament améliorant chez les humains avant d’avoir des preuves plus solides qu’il est efficace comme traitement dans différents types de modèles animaux de MH.
C’est aussi l’une des premières fois que le rôle du PPAR-delta a été étudié dans le cerveau, pour n’importe quelle maladie. Avant de lui donner un boost pharmaceutique pour une maladie cérébrale, il sera crucial de mieux comprendre son important rôle de coordination dans les cellules de tout le corps, y compris quelles autres protéines et voies il pourrait guider et diriger.
Néanmoins, si le KD3010 résiste à plus d’expérimentation, il serait beaucoup plus facile de le transférer en clinique pour la MH, car nous savons déjà qu’il est sûr pour les humains. En attendant, l’étude des protéines régulatrices maîtresses qui sont pertinentes pour la MH continuera à promouvoir la découverte de traitements innovants – à la fois nouveaux et anciens.
En savoir plus
Pour plus d’informations sur notre politique de divulgation, consulte notre FAQ…


