
Le silençage génique par ASO atteint plus loin et dure plus longtemps
Le silençage du gène de la huntingtine à l’aide de médicaments ASO atteint plus loin, dure plus longtemps et est sûr. Essai clinique humain bientôt ?
Les médicaments appelés oligonucléotides antisens, ou ASO, constituent un moyen de faire taire le gène qui cause la maladie de Huntington. Une nouvelle publication dans la revue Neuron suggère que le silençage génique par ASO atteint plus loin dans le cerveau que d’autres méthodes, dure plus longtemps et est sûr.
Nous attendions avec impatience les développements dans le domaine du silençage génique, et nous étions donc super excités de lire une nouvelle recherche majeure publiée aujourd’hui dans la revue de premier plan Neuron. Un groupe de chercheurs, dirigé par le Dr Don Cleveland à l’Université de Californie San Diego, en collaboration avec les compagnies pharmaceutiques Isis pharmaceuticals, Genzyme et Novartis, ont développé des oligonucléotides antisens (ASO) pour la maladie de Huntington. Alors, qu’ont-ils fait et qu’ont-ils découvert ?
Rappel génétique

Crédit image : www.biocomicals.com par Alper Uzun, PhD
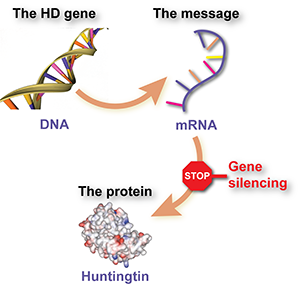
Le gène de la maladie de Huntington n’est qu’un parmi environ 25 000 paires de gènes, composés d’ADN, qui portent le code pour fabriquer les protéines ; les éléments constitutifs des cellules qui composent nos corps. Il y a quelques étapes entre le « code » ADN et la protéine finie. Une de ces étapes implique l’ARN messager, ou ARNm.
Le gène HD est le code qui, une fois traduit, produit l’ARNm HD. C’est l’ARNm qui dit à une cellule comment fabriquer la protéine huntingtine. Les personnes qui ont la maladie de Huntington ont une copie normale et une copie élargie du gène, donc elles fabriquent aussi deux types différents d’ARNm.
Depuis que le gène HD a été identifié, il y a près de 20 ans, les scientifiques ont essayé de comprendre ce qu’il fait, comment il cause les symptômes de la HD et comment l’éteindre efficacement.
Éteindre le gène
Il existe plusieurs méthodes possibles pour éteindre le gène HD. Peut-être la plus largement connue est l’interférence ARN, aussi connue sous le nom de RNAi ou parfois siRNA.
Une autre approche utilise une molécule légèrement différente appelée oligonucléotides antisens, ou ASO.
Les ASO sont un peu comme un croisement entre l’ADN et l’ARNm. Ils sont chimiquement similaires à l’ADN, mais sont constitués d’un seul brin comme l’ARNm. Tout comme les autres médicaments de silençage génique, ils sont conçus pour se coller à l’ARNm HD et dire à la cellule de le détruire, empêchant ainsi la protéine huntingtine anormale d’être jamais fabriquée.
La théorie derrière ceci est que si tu empêches la protéine huntingtine anormale d’être fabriquée, tu empêches ses effets dommageables sur les cellules, et donc tu réduis ou retardes les symptômes.
Au cours des derniers mois, nous avons entendu de bonnes nouvelles de plusieurs groupes travaillant sur les médicaments RNAi, mais jusqu’à récemment, les chercheurs ASO n’avaient pas publié autant. Cela vient de changer avec cette dernière publication, qui nous met à jour avec plusieurs années de travail acharné.
Les essais cliniques humains d’ASO dans d’autres maladies neurologiques ont déjà commencé, mais la situation dans la HD a été ralentie par quelques questions sans réponse.
L’effet des ASO
Dans ce tout nouveau travail, un groupe intelligent de chercheurs a examiné les effets de l’utilisation des ASO dans 3 modèles de souris différents de la HD, et aussi dans un modèle de singe (la meilleure chose après les humains en termes de modèles animaux), pour essayer de trouver les réponses à plusieurs questions différentes.
« Les ASO traitent des parties du cerveau que d’autres techniques de silençage génique n’ont pas pu atteindre »
Chez les singes, le médicament a été injecté dans le liquide spinal – une procédure beaucoup moins invasive que de l’injecter dans le cerveau, et une qui serait préférable pour les patients humains.
1. Que se passe-t-il quand tu perfuses un ASO, et combien de temps cela dure-t-il ?
Eh bien, ils ont perfusé les ASO dans les ventricules cérébraux (espaces remplis de liquide dans le cerveau) pendant deux à trois semaines. Cela a conduit à des niveaux diminués de la protéine huntingtine anormale dans de nombreuses zones connues pour être importantes dans le cerveau, y compris le striatum, qui est affecté le plus prominemment dans la maladie de Huntington. Les ASO ont pu se répandre beaucoup plus loin dans le cerveau que ce que nous avons vu avec les médicaments RNAi.
De plus, les niveaux sont restés bas pendant longtemps – jusqu’à trois mois après l’arrêt de la perfusion.
2. Qu’est-il arrivé aux symptômes ?
Les chercheurs sont capables de surveiller les symptômes des modèles animaux en utilisant des tests qui mesurent les mouvements et le comportement. Les animaux traités avec des ASO se sont améliorés par rapport à leurs homologues non traités. Encore mieux, l’amélioration a été soutenue pendant longtemps – et pas seulement pendant que les niveaux de protéine restaient bas. Les symptômes étaient encore meilleurs quelques mois après que les niveaux de protéine huntingtine anormale soient revenus aux niveaux d’avant traitement.
Cela soutient l’idée que le cerveau peut n’avoir besoin que d’un peu d’assistance, pour l’aider à survivre aux effets du gène HD. Un chercheur HD éminent, Carl Johnson, a inventé le terme « vacances de huntingtine » pour suggérer qu’une courte pause de la protéine nocive pourrait être tout ce qui est nécessaire pour faire pencher la balance en faveur de la récupération.
3. Quand est le meilleur moment pour donner le traitement ?
Cette étude suggère que le traitement précoce est probablement meilleur.
Les symptômes moteurs dans un modèle de souris particulier se sont améliorés dans le mois suivant le traitement, et ont continué à s’améliorer jusqu’à ce que les souris HD ne semblent pas différentes des souris normales. Les symptômes comportementaux ont été restaurés à la normale dans les 2 mois suivant le traitement.
Quand des souris plus âgées avec plus de symptômes ont été traitées, leurs symptômes moteurs et comportementaux se sont améliorés, mais il a fallu beaucoup plus de temps pour que les améliorations soient perceptibles, et elles n’ont pas récupéré autant que les souris plus jeunes et en meilleure santé.
4. Que se passe-t-il si tu bloques l’ARNm HD « normal » ?
C’est l’une des principales questions qui nous retiennent de commencer les essais dans la maladie de Huntington. Nous savons que la protéine huntingtine est essentielle pour le développement précoce, car les embryons de souris conçus pour ne produire aucune huntingtine meurent avant leur naissance. Est-il sûr d’éteindre la production de la protéine huntingtine normale et anormale chez les adultes ?
Grâce à ce travail, et au travail d’autres chercheurs en silençage génique, nous nous rapprochons d’une réponse. Éteindre l’ARNm HD normal pendant jusqu’à 3 mois chez des singes en bonne santé a été bien toléré. Dans les modèles animaux de HD, éteindre à la fois l’ARNm normal et anormal n’a pas changé la quantité de récupération et n’a eu aucun mauvais effet.
Le seul point d’achoppement possible maintenant, c’est que les humains peuvent être plus sensibles à avoir moins de huntingtine que n’importe quel animal sur lequel nous pourrions tester les médicaments. Seul un essai avec des patients nous le dira avec certitude.
Ce sont toutes de bonnes nouvelles
Nous avons maintenant la preuve que les ASO traitent des parties du cerveau que d’autres techniques de silençage génique n’ont pas pu atteindre. Non seulement cela, mais une perfusion à court terme avec des ASO a été suffisante pour retarder la progression des symptômes dans les modèles animaux de la maladie de Huntington. Et l’inversion des symptômes dure beaucoup plus longtemps que prévu, même après que les niveaux de la protéine huntingtine anormale reviennent à la normale.
Que se passe-t-il ensuite ?
Nous savons que les personnes qui portent le gène HD élargi peuvent rester parfaitement en bonne santé pendant de nombreuses années, malgré la production de la protéine huntingtine anormale depuis la naissance.
Peut-être qu’un traitement unique avec des ASO, ou un traitement une fois par an, sera suffisant pour « remettre à zéro l’horloge de la maladie » en bloquant la production de la protéine huntingtine assez longtemps pour laisser les cellules éliminer l’accumulation. La prochaine étape dans la recherche de ce groupe sera d’examiner combien de temps durera une seule injection d’ASO.
Ce travail suggère aussi que la perfusion dans le liquide spinal pourrait être assez bonne pour les médicaments ASO. Ce n’est pas une promenade de santé, mais c’est relativement simple comparé à l’installation de tubes et de pompes pour faire parvenir les médicaments directement dans le cerveau.
Nous devons aussi déterminer combien d’ASO sera nécessaire pour produire un effet chez les humains, quand et pendant combien de temps il devrait être donné, et être préparés aux effets secondaires inattendus.
Mais il semble que nous nous rapprochons toujours plus des essais de silençage génique HD humain. Et avec plusieurs groupes différents tous au bord des essais, et impatients d’être les premiers à tester leur médicament chez les patients, c’est vraiment une période excitante pour le silençage génique dans la HD.
En savoir plus
Sources et références
Pour plus d’informations sur notre politique de divulgation, consulte notre FAQ…


