Nouvel outil passionnant de réduction de la huntingtine décrit
Nouveau travail passionnant de réduction de la huntingtine de @SangamoTx et @CHDIfoundation utilisant les « doigts de zinc » pour arrêter l’expression du gène de la huntingtine mutante. Plus de détails sur cette nouvelle technique passionnante ici.

Un nouvel outil passionnant dans la lutte contre la maladie de Huntington vient d’être décrit. Un groupe international de scientifiques a développé une nouvelle méthode ciblée pour réduire les niveaux de la protéine huntingtine mutante.
Génétique de la huntingtine : du gène à la protéine
La maladie de Huntington (MH) est causée par un changement génétique – ou mutation – dans l’ADN d’un gène spécifique. Les scientifiques appellent ce gène huntingtine. Comme tous les autres fragments d’ADN dans nos cellules, le gène de la huntingtine est composé de quatre lettres chimiques, qui se répètent selon des motifs uniques qui leur donnent leurs fonctions spécifiques.
Ces quatre lettres d’ADN sont désignées par des abréviations de leurs noms chimiques, « A », « C », « T » et « G ». Chaque cas de MH est causé par un allongement d’une longue séquence des lettres d’ADN « C-A-G » très près du début du gène de la huntingtine. Chez la plupart des gens – ceux qui ne sont pas destinés à développer la MH – ce code « C-A-G » est répété environ 20 fois, pour des raisons que nous ne comprenons pas encore totalement.
La MH survient quand une personne hérite d’une séquence allongée de « C-A-G », la maladie apparaissant inévitablement chez les personnes qui héritent de 40 « C-A-G » ou plus. Note que tout le monde a deux copies différentes du gène de la huntingtine – une héritée de maman et une de papa. La grande majorité des patients MH ont une copie normale avec un faible nombre de « C-A-G », et la copie mutante dans laquelle ils sont plus longs.
La plupart des gènes, y compris le gène de la huntingtine, sont utilisés par les cellules comme manuels d’instructions pour construire des protéines – de minuscules machines moléculaires qui aident les cellules à faire leur travail. Donc dans les cellules des personnes avec la mutation MH, il y a deux versions différentes du gène de la huntingtine, et ces instructions disent à la cellule de fabriquer deux versions différentes de la protéine huntingtine.
Réduction de la huntingtine
Un objectif majeur du monde de la recherche sur la MH actuellement est d’étudier si les stratégies de « réduction de la huntingtine » pourraient être des traitements efficaces pour la MH. L’objectif des traitements de réduction de la huntingtine est d’arrêter, ou de ralentir, la vitesse à laquelle les cellules utilisent l’information dans le gène de la huntingtine pour fabriquer la protéine huntingtine.
Les études animales suggèrent que si nous pouvons réduire la quantité de protéine huntingtine fabriquée à partir du gène de la huntingtine mutante, nous pourrions avoir l’espoir de réduire les symptômes de la MH. Un certain nombre de compagnies pharmaceutiques utilisent une large gamme d’approches pour réduire la huntingtine comme nouveaux traitements potentiels pour la MH. Nous avons couvert l’idée générale de la réduction de la huntingtine ici, avec des mises à jour plus récentes sur les médicaments de réduction de la huntingtine appelés ASO ici et ici, et d’autres approches ici et ici.
Et maintenant, les ZFP
La compagnie de biotechnologie Sangamo Therapeutics travaille depuis plusieurs années sur encore une autre façon de réduire les protéines : en contrôlant si un gène est activé ou non. Leur technologie repose sur de petites machines moléculaires appelées facteurs de transcription à doigts de zinc. C’est un peu compliqué à dire, donc nous les appellerons simplement ZFP pour faire court. Tout comme les autres technologies de réduction de la huntingtine que nous avons décrites avant, l’objectif pour les chercheurs utilisant les ZFP dans la MH est de réduire les niveaux de huntingtine dans les cellules.
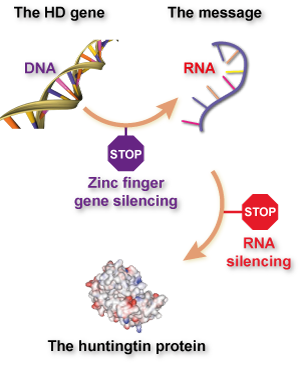
Bien que l’idée de base soit la même, les ZFP fonctionnent d’une manière assez unique, comparés aux technologies existantes de réduction de la huntingtine. Les médicaments existants de réduction de la huntingtine fonctionnent en ciblant une étape intermédiaire entre la lecture de l’information du gène de la huntingtine à partir de l’ADN et la fabrication de la protéine huntingtine. L’information dans les gènes est d’abord lue à partir de l’ADN, copiée dans un langage étroitement apparenté appelé ARN puis traduite dans le langage des protéines. Ce message ARN intermédiaire est la cible des médicaments de réduction de la huntingtine actuellement en clinique.
Mais les ZFP, comme ceux développés par Sangamo et leurs collaborateurs, fonctionnent d’une manière très différente. Nos cellules contiennent un certain nombre de protéines qui incluent de minuscules petites pinces, qui sont façonnées juste comme il faut pour saisir des séquences d’ADN spécifiques. (Alerte geek – les pinces sont maintenues ensemble par un atome de zinc, ce qui explique le nom bizarre).
« Contrairement aux approches qui ciblent l’ARN de la huntingtine, les cellules traitées avec des ZFP n’activent jamais leur gène de la huntingtine en premier lieu. »
ZFP pour la MH ?
Pendant de nombreuses années, les chercheurs ont travaillé pour comprendre les ZFP naturels dans l’espoir qu’ils pourraient les reprogrammer pour s’attacher à de nouvelles séquences d’ADN spécifiques. Sangamo a été un leader dans ce domaine, et a développé une sorte de boîte à outils de ZFP personnalisés qui peuvent cibler presque n’importe quelle séquence d’ADN.
Pourquoi faire cela, quel est l’intérêt de fabriquer des pinces personnalisées qui se lient à l’ADN ? Eh bien, il s’avère que nous pouvons attacher diverses charges utiles à ces pinces, et certaines d’entre elles font des choses très intéressantes à l’ADN où elles s’attachent. Par exemple, les chercheurs savent qu’ils peuvent fusionner une sorte de panneau d’arrêt cellulaire aux doigts de zinc, pour empêcher la cellule d’activer le gène ciblé.
Une publication récente décrit le travail de Sangamo développant des ZFP pour utilisation dans la MH, qui était une collaboration à grande échelle avec la fondation CHDI et un certain nombre de chercheurs MH autour du monde. Après un effort de criblage laborieux, ils ont pu développer de nouveaux ZFP qui s’attachent au gène de la huntingtine – dans l’ADN – et bloquent son activation. Donc, contrairement à d’autres approches qui ciblent l’ARN de la huntingtine, les cellules traitées avec ces ZFP n’activent jamais leur gène de la huntingtine en premier lieu.
Encore mieux, l’équipe a pu développer des ZFP qui peuvent arrêter l’expression de seulement la copie mutante du gène de la huntingtine, tout en laissant la copie normale entièrement tranquille. Sangamo a testé leur capacité à discriminer entre une des plus petites tailles de CAG qui causent la MH chez les humains (38 répétitions CAG), tout en laissant la copie normale de huntingtine tranquille.
Résultats prometteurs chez les souris
Ayant prouvé dans les cellules que leurs nouveaux ZFP pouvaient arrêter spécifiquement la huntingtine mutante, l’équipe a ensuite fait un certain nombre d’études animales très bien menées pour voir si leur outil pourrait être utile dans les cerveaux d’animaux qui ont des mutations similaires à la MH. Pour être complets, ils ont testé deux modèles animaux différents de MH – un avec des symptômes progressant très rapidement, et un autre avec des changements à long terme plus subtils.
Dans les deux cas, la livraison de ZFP aux cerveaux de souris a mené à des réductions de la protéine huntingtine. Cela a aussi aidé certains des symptômes que ces souris éprouvent, qui ressemblent un peu aux choses que nous observons chez les patients MH.
Il est raisonnablement facile de tester des médicaments expérimentaux comme celui-ci chez les souris. Les chercheurs sont capables de collecter du tissu cérébral d’animaux et de l’étudier intensivement, mais des études similaires sont impossibles chez les patients MH humains, qui deviennent assez grincheux si tu prends des morceaux de leur cerveau. Parce que traduire les études de souris en humains est si difficile, l’équipe a fait un autre ensemble d’expériences pour déterminer si le traitement ZFP améliorait les choses d’une manière que nous pouvons aussi mesurer chez les gens.
En fait, utilisant des techniques sophistiquées de scan cérébral, l’équipe a pu observer des bénéfices du traitement ZFP chez les souris MH. Ces techniques bien établies fonctionnent aussi chez les humains, donc si nous voulons tester les ZFP dans des études humaines nous pouvons espérer chercher des améliorations sans le besoin d’enlever du tissu.

Quels sont les risques et bénéfices des ZFP ?
Comme avec tous les autres traitements potentiels pour la MH, il y a des bénéfices et des désavantages à l’utilisation des ZFP. En théorie, c’est une bien meilleure approche d’arrêter la production de protéine d’un gène mutant entièrement, plutôt que d’essayer de nettoyer l’ARN et la protéine après coup. Nous ne comprenons pas complètement quelles espèces d’ARN et de protéine ont des effets toxiques dans les cellules, donc l’arrêter à la source semble être la meilleure approche.
De plus, les données présentées par Sangamo et leurs collaborateurs montrent une très belle capacité à discriminer entre la copie normale du gène de la huntingtine et la copie mutante. Faire taire juste la copie mutante du gène de la huntingtine et épargner l’autre copie est, en théorie, préférable, puisque nous ne connaissons toujours pas tous les risques associés à la réduction de la copie normale.
Du côté négatif, les ZFP développés par Sangamo et leurs collaborateurs sont des gènes eux-mêmes, encodés dans l’ADN, qui doivent être livrés à chaque cellule que nous voulons traiter. Utiliser la livraison de gènes pour traiter une maladie est généralement connu comme thérapie génique. Pour être un traitement efficace pour la MH, la thérapie génique ZFP nécessitera certaines interventions. L’ADN encodant les ZFP doit être emballé dans un virus et injecté dans le cerveau.
Comme tout médicament, les ZFP développés par Sangamo et leurs collaborateurs pourraient avoir des conséquences inattendues. Dans ce cas, la préoccupation la plus simple concernant les ZFP pourrait être qu’ils ciblent accidentellement d’autres gènes – en plus de la huntingtine – pour la réduction. L’équipe a mené des investigations assez détaillées de cette possibilité dans les cellules, mais bien sûr dans le cerveau les choses pourraient être plus compliquées.
La meilleure façon de déterminer si ces ZFP sont aussi utiles que nous l’espérerions est de mener des études humaines. Pour soutenir cela, Sangamo a établi un partenariat avec le géant pharmaceutique japonais Takeda, qui a certainement l’expertise et les ressources pour mener de telles études. Reste à l’écoute de HDBuzz pour toute annonce concernant de futures études avec les ZFP chez les patients MH.
À retenir
Cette nouvelle étude passionnante fournit une autre flèche dans notre carquois alors que nous nous attaquons à la réduction de la huntingtine en clinique. L’étude était très bien menée, et nous laisse bien positionnés pour considérer tester les ZFP dans des études cliniques humaines. C’est très excitant de voir que des scientifiques brillants autour du monde continuent à développer de nouvelles approches pour traiter la MH.
Ces nouveaux ZFP semblent susceptibles de fournir des bénéfices excitants comparés à d’autres approches de réduction de la huntingtine que nous avons hâte de voir testées chez les patients MH. Reste à l’écoute de HDBuzz pour plus de couverture des thérapies de réduction de la huntingtine !
En savoir plus
Pour plus d’informations sur notre politique de divulgation, consulte notre FAQ…


