Une mise à jour confirme que l’essai de silençage génique dans le cadre de la maladie de Huntington est sur la bonne voie
Ionis annonce que son essai HTTRx (diminuer la protéine huntingtine), est complet et prévoit de l'étendre
 Par Dr Jeff Carroll 30 juin 2017 Edité par Dr Tamara Maiuri Traduit par Michelle Delabye & Dominique Czaplinski Initialement publié le 22 juin 2017
Par Dr Jeff Carroll 30 juin 2017 Edité par Dr Tamara Maiuri Traduit par Michelle Delabye & Dominique Czaplinski Initialement publié le 22 juin 2017
La compagnie Ionis Pharmaceuticals a lancé, à la fin de l’année 2015, le tout premier essai portant sur un médicament visant à diminuer la huntingtine, parfois appelé un ‘médicament de silençage génique’. Lors d’une mise à jour notable, la compagnie a annoncé deux étapes importantes : l’essai est à ce jour complet et une ‘étude de prolongation ouverte’ sera activée dans cet essai pour les volontaires. Bien que rien ne soit garanti, ceci laisse bien augurer de l’avenir de cet important programme.
Un rapide récapitulatif sur la diminution de la huntingtine
L’idée de ‘déconnecter’ l’origine de la maladie de Huntington était l’une des premières pensées venue à l’esprit des chercheurs lorsque le gène MH a été découvert en 1993.
Les premiers progrès importants dans la réalisation de cette idée sont arrivés il y a une dizaine d’années, lorsque plusieurs études sur la souris ont remporté un succès s’agissant de la diminution de l’activité du gène. Faire diminuer le taux de la protéine pour laquelle le gène est une recette : la huntingtine mutée. Dans chaque cas, la diminution de la huntingtine a amélioré les symptômes de la maladie chez les souris MH.
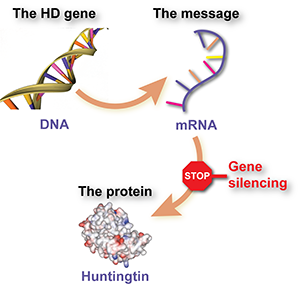
Ces médicaments de diminution de la huntingtine agissent tous de manière similaire, en ‘tuant le messager’. Un gène est une recette pour une protéine mais entre le gène et la protéine, un messager chimique est produit, lequel est essentiellement une copie de travail du gène. Le fait de se débarrasser du messager brise la chaîne de production, en conséquence, moins de protéines sont produites.
Ces médicaments sont produits à partir de molécules similaires à celles de l’ADN, les choses dont sont constitués nos gènes. Ces types de substances chimiques ont la particulière capacité à adhérer fermement les uns aux autres si la séquence de ‘lettres’ génétiques est correctement agencée. Les concepteurs de médicaments peuvent concevoir des molécules ayant une séquence qui adhèrera à la molécule messager du gène huntingtin et pas à d’autres messagers.
Lorsque la cellule voit que le messager a une molécule médicamenteuse collé à lui, elle décèle que quelque chose d’inhabituel s’est produit et réagit en supprimant la molécule messager. Finalement, cela diminue le taux de protéine.
Les molécules médicamenteuses viennent elles-mêmes de plusieurs atmosphères différentes. Certaines sont produites à partir de l’ARN (la chose dont est constitué le messager), alors que d’autres sont produites à partir de l’ADN (la chose dont sont constitués nos gènes).
Un mot rapide sur la terminologie. Beaucoup de personnes, en ce compris les rédacteurs de HDBuzz, désignent ces molécules comme étant des médicaments de ‘silençage génique’ ; ce qui suggère légèrement que nous essayons de désactiver totalement le gène, ce qui est probablement impossible et non souhaitable. Donc, vous nous entendrez de plus en plus les appeler des médicaments de ‘diminution de la huntingtine’. Nous utiliserons encore le terme de ‘silençage génique’ de temps à autre, afin que les personnes puissent trouver le dernier article à ce sujet sur Google, ce terme étant mieux connu.
L'essai actuel
La compagnie qui a commencé à travailler sur la MH il y a une dizaine d’année et qui est à l’origine de l’essai actuel est une compagnie basée en Californie, dénommée Isis Pharmaceuticals. Il y a eu des changements depuis, en ce compris le nom de la compagnie qui depuis 2015 s’appelle Ionis.
Le médicament de Ionis est un oligonucléotide antisens, ou ASO. Il s’agit d’un seul brin d’ADN chimiquement modifié, conçu pour adhérer à la molécule messager issue du gène huntingtin.
Juste pour garder les choses passionnantes, le médicament lui-même s’appelait initialement ISIS-443139 mais dernièrement, il a eu pour nom IONIS-HTTRx ou seuelement HTTRx - une combinaison de HTT, l’abréviation scientifique utilisée pour le gène huntingtin, et Rx, un symbole utilisé dans l’industrie pharmaceutique pour signifier un traitement ou une prescription.
«L'étude de prolongation ouverte ne sera disponible que pour les participants de l'essai en cours. »
(Fait amusant: l'origine de ‘Rx’ est inconnue, mais elle peut provenir du mot latin ‘recette’).
L’essai de Ionis, mené en partenariat avec le Professeur Sarah Tabrizi de l’Univiersity College London, était le tout premier essai au cours duquel un médicament visant à diminuer la huntingtine était testé chez les humains. Comme dans tout premier essai concernant un nouveau médicament, le principal objectif est l’innocuité.
Pour atteindre le cerveau, les médicaments ASO, tels que HTTRx, doivent être injectés dans le liquide cérébro-spinal en utilisant une mince aiguille. Cela s’appelle l’injection intrathécale. Bien que cette méthode puisse paraître horrible, celle-ci est fréquemment utilisée pour le traitement du cerveau dans d’autres situations, telles que le cancer. Une méthode étroitement liée, la ponction lombaire ou rachicentèse, est très largement utilisée, et en effet, de nombreux bénévoles issus de familles MH ont subi cette méthode afin de faire don de liquide cérébro-spinal, précieux pour la recherche MH.
L’actuel essai d’innocuité HTTRx implique des patients présentant les premiers symptômes de la maladie de Huntington. Après une évaluation clinique approfondie, chaque volontaire reçoit quatre injections du médicament à intervalles mensuels, suivies d’une collecte finale du liquide cérébro-spinal.
Tout au long de l’essai, un groupe placebo a été utilisé afin de distinguer les effets du médicament des effets en cours dans l’essai, comme pour la méthode d’injection. L’essai a un protocole d’intensification de la dose : de très faibles doses ont été administrées au début, les volontaires recevant plus tard des doses plus élevées.
Quoi de neuf ?
Le communiqué de presse du 22 juin 2017 de Ionis, première mise à jour officielle depuis le début de l’essai, apporte prudemment des nouvelles optimistes. Il contient deux annonces importantes. Premièrement, le recrutement dans l’essai actuel est terminé. Et deuxièmement, la compagnie lance une étude de prolongation ouverte pour l’essai en cours.
L’achèvement du recrutement est une étape importante pour tout essai, mais pour celui-ci, il est particulièrement important. L’essai a impliqué un certain nombre de « premières » - le premier médicament ASO administré chez des patients MH, la première fois qu’une injection intrathécale est utilisée dans le cadre de la MH – et chaque intensification du dosage a apporté l’espoir d’avantages positifs et un risque accru d’effets indésirables.
Tout au long d’un tel essai, un comité indépendant d’experts examine régulièrement toutes les données de sécurité pour rechercher un signe de danger ou de lésions. Les informations sur le fait que le recrutement de l’essai est terminé et que les patients finaux ont accompli les procédures suggèrent fortement que même aux doses les plus élevées, l’innocuité du médicament semble bonne. Malgré des tests de sécurité exhaustifs avant d’être testé chez des patients, tout médicament peut produire des effets indésirables ; ce sont donc les meilleures nouvelles que nous pouvions espérer entendre à ce stade.
Selon les termes du communiqué de presse : “Le profil d’innocuité et de tolérance de Ionis-HTTRx dans l’étude de cohortes Phase 1/2a soutient son développement continu”. Nous y sommes parvenus.

Avec un recrutement complet, Ionis est maintenant en mesure de définir un calendrier pour l’achèvement de l’essai et pour une première version de ses résultats. “Les premiers résultats” sont attendus vers la fin de l’année 2017. Selon notre expérience, les résultats d’un tel essai peuvent ne pas tous sortir en une seule fois. Les données d’innocuité peuvent être les premières à être publiées, mais les informations sur le fait de savoir si le traitement avec HTTRx a diminué le taux de la protéine huntingtine dans le liquide cérébro-spinal – un résultat ‘biomarqueur’ très attendu – peuvent prendre plus de temps pour se matérialiser.
Une étude de prolongation ouverte
L’essai HTTRx actuel se déroule en aveugle : certains volontaires ont reçu quatre injections ne contenant aucun médicament actif et ni les patients, ni le personnel de l’essai ne savaient qui recevait le médicament ou le placebo.
Dans le cadre d’une étude de prolongation ouverte, ou OLE, les volontaires de l’essai en aveugle sont invités à revenir pour d’autres doses, et chaque volontaire reçoit le médicament actif, plutôt que certains reçoivent un médicament et certains le placebo – généralement la dose la plus élevée testée en toute sécurité lors de l’essai en aveugle.
Ionis avait précédemment annoncé qu’une étude de prolongation ouverte pourrait être mise en œuvre si les données sur la sécurité de l’essai semblaient bonnes. Nous ne voulons pas trop en déduire de cette brève annonce, mais dans la mesure où l’exécution d’une étude de prolongation ouverte est coûteuse pour un sponsor d’essai, cette annonce nous apporte donc certainement de l’optimisme s’agissant de l’ensemble du programme HTTRx.
L’étude de prolongation ouverte sera seulement disponible pour les volontaires de cet essai. Ce qui signifie qu’elle aura lieu dans les mêmes centres actuels situés au Royaume-Uni, Canada et Allemagne. La durée ainsi que la description exacte de l’OLE n’ont pas encore été annoncées mais engendra une quantité impressionnante d’informations que Ionis et son partenaire, Roche pourront utiliser pour planifier les étapes suivantes.
Remerciements à nos héros
Un avantage important de l’étude de prolongation ouverte est qu’elle récompense les volontaires qui ont participé à l’étude initiale en leur donnant un accès garanti au médicament actif. Nous sommes particulièrement ravis de cet aspect de l’annonce. Les participants à cet essai étaient tous des membres de familles MH qui ont sacrifié beaucoup de leur temps pour recevoir des injections dans la colonne vertébrale un médicament qui, au début de l’essai, n’avait jamais été auparavant administré chez des humains. Ceux qui ont été recrutés plus tard ont reçu des doses plus élevées que celles déjà administrées à d’autres.
Quelque soit le résultat, ces volontaires ont accepté des risques personnels, et dans la plupart des cas, pour aider les autres plutôt qu’eux-mêmes. Toute notre communauté doit à ces héros une grande gratitude pour leur bravoure et leur service. Joignez-vous à nous pour les saluer sur les médias sociaux en utilisant le hashtag #HDResearchHeroes.
Et après ?
«Ionis déclare : “la prochaine étape de ce programme sera de mener une étude pour déterminer si la diminution de la protéine huntingtine mutante avec IONIS-HTTRx peut ralentir la progression de cette terrible maladie”. »
L’étude de prolongation ouverte va bientôt commencer, probablement dans les prochains moins. Les volontaires de l’essai d’innocuité vont être contactés par les sites d’étude pour être informés sur comment et quand ils peuvent s’inscrire à cette étude. Pendant ce temps, les participants qui sont encore dans l’essai en aveugle devront terminer leur participation avant de passer à l’étude de prolongation ouverte.
Si vous ne participiez pas à l’essai en aveugle, vous ne pouvez pas vous inscrire à l’étude de prolongation ouverte. Merci de ne pas contacter les sites d’étude, sauf si vous participiez à l’essai initial.
Vers la fin de l’année 2017, nous pouvons nous attendre à entendre une annonce officielle concernant les résultats de l’essai en aveugle. Ne soyez pas déçus si celle-ci se limite aux données de sécurité en première instance. “Sûr et bien toléré” devrait être la musique aux oreilles des membres des familles MH après un essai de ce genre !
Plus tard, peut-être au début de l’année 2018, il peut y avoir une annonce distincte sur certains des résultats plus expérimentaux de l'essai d’innocuité - des choses telles que HTTRx a diminué le niveau de huntingtine dans le liquide cérébro-spinal.
La prochaine grande nouvelle, si tout continue d'aller bien, peut être une annonce portant sur un essai d'efficacité pour tester le médicament HTTRx sur une durée suffisante afin de déterminer s’il ralentit la progression de la maladie. La Compagnie Roche a maintenant le droit d'opter pour la prise en charge du développement du médicament et d'exécuter un tel essai en fonction de son propre processus décisionnel. Avec un peu de chance, nous pourrons peut-être en entendre parler dans les mois à venir.
Insistant sur leur désir de faire avancer le médicament, la compagnie a, dans une annonce distincte faite directement à la communauté MH, déclaré: “Après l'achèvement de l'étude, la prochaine étape de ce programme sera de mener une étude pour déterminer si la diminution de la protéine huntingtine mutante avec IONIS-HTTRx peut ralentir la progression de cette terrible maladie”.
Nous ne savons pas encore quand la prochaine grande étude commencera, mais notre meilleure hypothèse pourrait être à la fin de l’année 2018 ou au début de l’année 2019. Quant à la date, au nombre de patients et aux pays et sites concernés, il est trop tôt pour être sûr, mais la compagnie Ionis déclare : “De futures études pour le programme seront menées à l'échelle mondiale et comprendront des sites d'étude américains”. En ce qui concerne le reste, vous pouvez être sûrs d’en savoir plus en consultant le site HDBuzz.
Rien ne se passe assez rapidement pour les personnes dont les familles sont touchées par la maladie de Huntington, mais c'est un moment pour faire une pause et être ravis de savoir que, pour cet important programme de diminution de la huntingtine, les nouvelles sont jusqu’à présent toutes bonnes.


