
Des avancées sur de nombreux fronts dans la lutte contre la protéine responsable de la maladie de Huntington
Cet automne, plusieurs entreprises axées sur de nouvelles technologies de réduction de la huntingtine, dont Wave, PTC et Voyager, font des annonces passionnantes

Nous avons eu une série de mises à jour passionnantes d’Ionis et Roche/Genentech concernant leur programme de test d’un médicament qui réduit la production de la protéine huntingtine – mais ils ne sont plus les seuls sur le marché. Récemment, plusieurs autres acteurs – dont Wave Life Sciences, PTC Therapeutics et Voyager Therapeutics – ont fait de grandes annonces concernant leurs propres programmes de réduction de la huntingtine. Il se passe beaucoup de choses, et HDBuzz est là pour t’aider à démêler toutes ces approches.
Réduction de la huntingtine
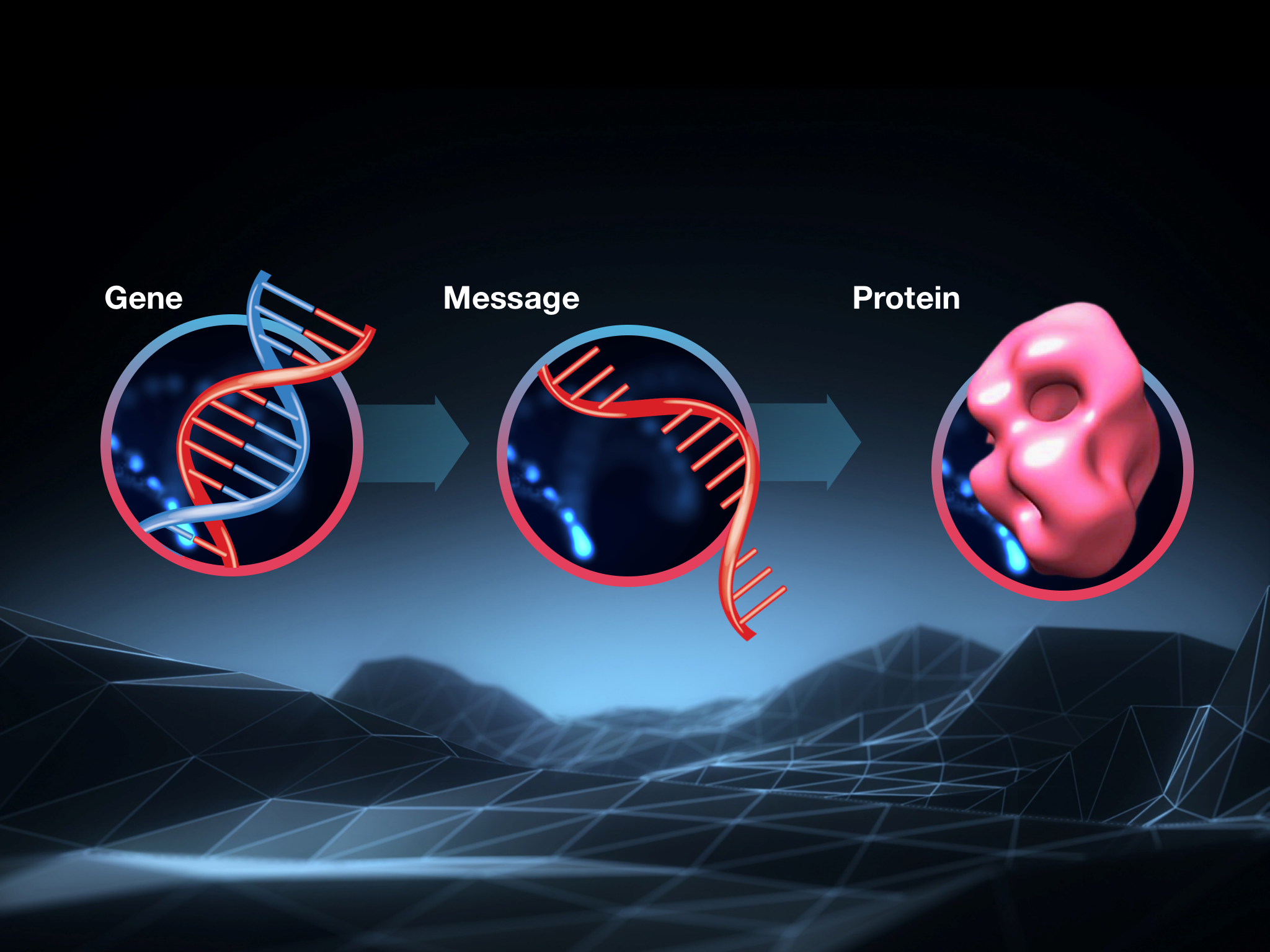
L’objectif, pour toutes ces approches, est de réduire la quantité de protéine huntingtine dans les cellules du cerveau. La protéine huntingtine est la petite machine fabriquée par les cellules lorsqu’elles suivent le plan trouvé dans le gène HD. C’est la protéine huntingtine mutante, et non la mutation dans l’ADN, que la plupart des chercheurs pensent être responsable du dysfonctionnement des cellules cérébrales qui cause la MH.

Un petit rappel sur le fonctionnement de ce processus s’impose avant d’entrer dans le vif du sujet. Les cellules suivent les instructions trouvées dans l’ADN, mais elles ne l’utilisent pas directement pour fabriquer une protéine : elles copient les instructions trouvées dans l’ADN dans une sorte de copie de brouillon de l’information génétique, faite à partir d’un produit chimique étroitement apparenté appelé ARN. Les scientifiques appellent cette copie de brouillon ARN messager ou ARNm en abrégé.
Ainsi, les instructions du gène HD, dans notre ADN, sont copiées en ARN messager, qui est ensuite interprété par la cellule pour construire la protéine huntingtine. Un peu déroutant, mais ça marche !
Si tu ne retiens qu’une seule chose, retiens ceci : une rupture dans la chaîne, où que ce soit, empêchera les cellules de fabriquer la protéine huntingtine. Dans les études sur les animaux, la réduction de la protéine huntingtine a conduit à de grandes améliorations des symptômes similaires à ceux de la MH.
Cette approche thérapeutique de la MH est appelée réduction de la huntingtine et elle est à la base du programme Ionis/Roche et du prochain grand essai de phase 3. Récemment cependant, au moins trois autres entreprises ont annoncé des avancées passionnantes dans diverses approches de réduction de la huntingtine.
L’approche ciblée de Wave
« L’approche de Wave cible de minuscules différences génétiques entre les gènes HD sains et mutants, en dehors de la séquence CAG responsable de la maladie. Ces petites différences d’orthographe font partie de la variation génétique humaine normale et ne semblent avoir aucun impact sur les symptômes de la MH. Mais ces minuscules différences d’orthographe fournissent une cible pour un ASO qui peut faire la distinction entre le message HD normal et le message mutant. »
Tout d’abord, il y a non pas un, mais deux essais de Wave Life Sciences. Nous avons écrit sur l’approche de Wave
Comme dans l’essai Ionis/Roche, Wave cible le message de la huntingtine pour le détruire dans l’espoir d’améliorer les symptômes de la MH. Mais Wave adopte une approche légèrement différente. Rappelle-toi que pratiquement chaque patient atteint de la MH a un gène HD mutant et une copie normale. Le médicament Ionis/Roche cible les deux copies, réduisant finalement les niveaux de la protéine Huntingtine normale et mutante dans le cerveau.
L’approche de Wave cible de minuscules différences génétiques entre les gènes HD sains et mutants, en dehors de la séquence CAG responsable de la maladie. Ces petites différences d’orthographe font partie de la variation génétique humaine normale et ne semblent avoir aucun impact sur les symptômes de la MH. Mais ces minuscules différences d’orthographe fournissent une cible pour un ASO qui peut faire la distinction entre le message HD normal et le message mutant.
Dans un monde parfait, cibler uniquement le gène HD mutant est évidemment préférable. Le gène HD normal a un certain nombre de rôles importants dans les cellules, que nous ne comprenons pas tous parfaitement. S’il était tout aussi facile de supprimer uniquement la copie mutante, c’est ce que nous devrions faire.
Cependant, il y a toujours un compromis. Pour la réduction de la huntingtine, le compromis est que tous les patients atteints de la MH ne sont pas éligibles aux ASO développés par Wave. Pour que leur approche fonctionne, une personne doit avoir hérité de la mutation HD et aussi de l’une des différences d’orthographe génétique sur lesquelles les médicaments se concentrent.
Wave a mené des études dans des cliniques MH et a montré que jusqu’à environ deux tiers des patients atteints de la MH pourraient être traités avec l’un des deux ASO qu’ils ont développés. Chacun d’eux cible une variation génétique différente, et avoir deux médicaments leur permet d’utiliser leur approche sur une plus grande partie de la population MH.
Ils testent la sécurité de ces deux premiers ASO de réduction de la huntingtine mutante chez des patients atteints de la MH au Canada, en Europe et aux États-Unis. Comme le premier essai Ionis/Roche, l’objectif de ces études est de déterminer si ces médicaments sont sûrs. Si c’est le cas, ils seraient ensuite testés pour leur capacité à améliorer les symptômes de la MH dans des études plus importantes.
Nous avons également récemment appris de Wave qu’ils travaillent en coulisses sur un autre ASO, ciblant encore une autre variation du gène HD. Ce troisième médicament n’est pas encore testé chez l’homme, mais il offre un espoir supplémentaire aux personnes qui ne sont pas éligibles pour l’un ou l’autre des médicaments Wave existants. En 2019, nous espérons entendre des mises à jour préliminaires sur les études de sécurité humaine des deux premiers essais Wave, ainsi que plus de détails sur leur programme de développement d’un troisième ASO.
Qu’est-ce que le P-T-C ?
Ce ne sont pas seulement les ASO dans le monde de la réduction de la huntingtine. Lors de la réunion du Réseau européen de la maladie de Huntington à Vienne cet automne, Anu Bhattacharyya, de PTC Therapeutics, a informé le public de l’EHDN des progrès passionnants réalisés dans son entreprise, qui s’intéresse également à la réduction de la huntingtine comme traitement de la MH.
« PTC développe ce que les chercheurs appellent une petite molécule, c’est-à-dire un médicament qui peut, espérons-le, être pris sous forme de pilule, pour réduire les niveaux de l’ARN messager de la huntingtine. Il y a quelques années, cela aurait semblé relever de la science-fiction, mais plusieurs entreprises ont décrit des médicaments expérimentaux où cette approche semble fonctionner. »
L’approche adoptée par PTC est totalement différente de l’approche ASO adoptée par Wave et Ionis/Roche. Tous les autres programmes impliquent des injections dans le cerveau ou la colonne vertébrale – utiles si elles fonctionnent, mais beaucoup plus invasives que ce que nous aimerions voir en fin de compte. PTC développe ce que les chercheurs appellent une petite molécule, c’est-à-dire un médicament qui peut, espérons-le, être pris sous forme de pilule, pour réduire les niveaux de l’ARN messager de la huntingtine. Il y a quelques années, cela aurait semblé relever de la science-fiction, mais plusieurs entreprises ont décrit des médicaments expérimentaux où cette approche semble fonctionner.
PTC est à l’avant-garde des entreprises développant cette nouvelle approche d’interférence avec des ARN messagers spécifiques, et ils ont les yeux rivés sur la MH. Ils ont développé un médicament qui réduit les niveaux de la protéine Huntingtine dans les cellules. Pour la première fois, à l’EHDN, Bhattacharyya a révélé que ces médicaments fonctionnent également dans le cerveau de souris vivantes – suggérant que les médicaments passent de l’estomac au cerveau, ce qui est une énorme réussite.
Ce qui est particulièrement cool, c’est que même si un médicament pris sous forme de pilule réduit la huntingtine dans le cerveau dans une moindre mesure qu’un médicament injecté, il pourrait quand même être vraiment utile. Une pilule de réduction de la huntingtine pourrait signifier que des injections spinales d’un médicament plus puissant ne seraient nécessaires que tous les six ou douze mois, par exemple, au lieu de tous les un ou deux mois.
Le programme de PTC en est à une phase plus précoce que les programmes Ionis/Roche et Wave, car il est encore testé sur des animaux. Mais c’est une approche vraiment passionnante qui pourrait offrir de réels avantages si elle s’avère sûre et efficace dans les futurs essais. Et PTC semble se préparer pour l’avenir – Bhattacharyya a dit au public de l’EHDN que PTC avait pour objectif de commencer des études de sécurité chez l’homme en 2020. Ce qui est excitant, c’est que PTC a un bilan de réussite, avec deux médicaments oraux approuvés pour la dystrophie musculaire, une autre maladie neurologique génétique.
Voyager
Lors d’une autre conférence cet automne – le Congrès de la Société européenne de thérapie génique et cellulaire – nous avons eu une autre mise à jour passionnante sur la réduction de la huntingtine de Voyager Therapeutics. Voyager est une entreprise de biotechnologie axée sur l’utilisation de la thérapie génique pour traiter les maladies du cerveau, y compris la maladie de Huntington.
La thérapie génique fonctionne très différemment des ASO ou des petites molécules. La thérapie génique repose sur de minuscules virus inoffensifs pour délivrer de nouvelles informations génétiques aux cellules – dans ce cas, aux cellules du cerveau. Les virus sont très doués pour s’infiltrer dans les cellules, alors des chercheurs astucieux ont trouvé comment les tromper pour qu’ils délivrent des choses bénéfiques dans différentes cellules du corps.
Dans ce cas, l’équipe de chercheurs de Voyager a construit des virus personnalisés qui délivrent des instructions qui indiquent aux cellules du cerveau comment fabriquer un morceau spécial d’ARN qui recherche l’ARNm de la huntingtine et le détruit. En effet, le virus reprogramme les cellules pour qu’elles deviennent des usines produisant un approvisionnement quotidien d’un médicament qui fonctionne comme les ASO dont nous avons parlé plus haut.
Cette approche présente un énorme avantage, à savoir que le traitement ne doit être administré qu’une seule fois. Une fois traitée, la cellule cérébrale produira théoriquement la molécule de réduction de la huntingtine indéfiniment. Si elle est sûre et efficace, cette approche serait évidemment préférable à des injections mensuelles dans le liquide céphalo-rachidien, ou même à la prise quotidienne d’une pilule.
Cependant, il y a quelques inconvénients potentiels à cette approche. Premièrement, elle pourrait s’avérer dangereuse d’une manière que nous ne pouvons pas prévoir à ce stade. Et comme le traitement n’est pas réversible, nous devons prendre des précautions supplémentaires en matière de sécurité pour les essais de thérapie génique. Deuxièmement, s’il est assez facile de faire pénétrer ces virus piratés dans la plupart des cellules d’un minuscule cerveau de souris, c’est beaucoup plus difficile de le faire dans les 86 milliards de neurones du cerveau humain.
« L’équipe de chercheurs de Voyager a mis au point des virus personnalisés qui fournissent des instructions aux cellules cérébrales pour fabriquer un élément spécial d’ARN qui recherche l’ARNm de la huntingtine et le détruit. En fait, le virus reprogramme les cellules pour qu’elles deviennent des usines de production quotidienne d’un médicament qui fonctionne comme les ASO dont nous avons parlé plus haut. »
C’est ce qui rend cette mise à jour des scientifiques de Voyager particulièrement intéressante. Ils ont fait état d’expériences menées sur des singes, qui ont de grands cerveaux complexes très proches des nôtres. Voyager a mis au point des techniques chirurgicales qui aident le virus à se propager sur de très grandes parties du cerveau du singe, tant dans les structures cérébrales profondes que dans le cortex, la partie externe ridée du cerveau.
Il s’agit d’une avancée particulièrement importante, car les structures cérébrales profondes ciblées par Voyager sont relativement mal atteintes par les médicaments ASO, mais jouent un rôle clé dans la MH. Les expériences de Voyager révèlent également une très bonne suppression du gène de la huntingtine chez le singe : des réductions d’environ deux tiers dans les structures cérébrales profondes et d’environ un tiers dans les cellules cérébrales corticales externes. Ce sont des réductions importantes, et l’on peut espérer que l’obtention de résultats similaires chez les patients humains atteints de la MH pourrait apporter de réels avantages.
Comme pour l’essai Ionis/Roche, la voie envisagée par Voyager consiste à réduire à la fois les copies mutantes et les copies normales du gène de la MH. Compte tenu de cela, et du fait que leur thérapie ne peut pas être interrompue après son administration, cette approche exige une approche très prudente, ce qu’ils semblent faire avec toutes ces études sur les singes.
À retenir
La communauté MH est très enthousiaste, à juste titre, au sujet de l’étude Ionis/Roche/Genentech en cours. Tout le monde, y compris HDBuzz, soutient cette étude et espère vivement qu’elle apportera des avantages aux patients atteints de la MH. Mais, comme le montrent ces récentes avancées, ce n’est pas le seul jeu en ville. Il existe d’autres approches pour réduire la huntingtine qui ne sont pas aussi avancées, mais qui offrent des avantages potentiels importants.
Pour résumer, il existe deux programmes d’essais en cours avec des ASO réduisant la huntingtine chez des patients. L’un cible les deux copies du gène de la MH (Roche/Genentech), a passé le test de sécurité et sera bientôt testé pour son efficacité. L’autre cible uniquement le gène mutant (Wave) et est actuellement testé pour sa sécurité. Derrière cela, nous avons des essais de thérapie génique à injection unique faisant l’objet d’études de sécurité approfondies en préparation des essais sur l’homme (Voyager et autres), et une approche à petite molécule vraiment novatrice (PTC).
Le fait de soutenir plusieurs tentatives n’augmente pas seulement les chances qu’une d’entre elles réussisse, mais offre également la possibilité que plus d’une fonctionne. Cela offre un avenir séduisant où des combinaisons de médicaments pourraient être utilisées pour produire un bénéfice maximal pour le risque le plus faible possible. Les approches combinées se sont avérées efficaces pour d’autres maladies comme le VIH, le cancer et le diabète. En ce qui concerne les médicaments en développement et les médicaments qui fonctionnent, plus il y en a, mieux c’est.
En savoir plus
Sources et références
Pour plus d’informations sur notre politique de divulgation, consulte notre FAQ…


